SAN MARCOS QUÍMICA PROBLEMAS RESUELTOS DE ADMISIÓN UNIVERSIDAD
PREGUNTA 1 :
En la tabla periódica de los elementos, una de las consecuencias de la configuración electrónica es el ordenamiento de los elementos en periodos y grupos. En el arreglo vertical se manifiestan las propiedades
A) físicas de los elementos que forman el periodo.
B) nucleares de los elementos que pertenecen al grupo.
C) nucleares de los miembros que tienen orbitales similares.
D) químicas de los elementos que forman el grupo.
E) físicas de los elementos que pertenecen al grupo.
RESOLUCIÓN :
En la tabla periódica, los elementos están ordenados en función al número atómico (en forma creciente) y a la configuración electrónica. Los elementos químicos se encuentran en arreglos verticales (grupos) y arreglos horizontales (periodos).
Periodo.
Los elementos presentan igual nivel de valencia (último nivel), además, sus propiedades físicas y químicas son diferentes.
Grupo.
Los elementos presentan igual número de electrones de valencia (electrones del último nivel); también presentan propiedades químicas similares pero propiedades físicas diferentes.
Los elementos de un mismo grupo tienen la misma distribución electrónica externa, por lo tanto, los elementos de una misma familia o grupo presentan propiedades químicas similares, porque cuando los átomos reaccionan para formar iones o moléculas, son los electrones más externos los que participan.
En conclusión, los elementos de un mismo grupo tienen mismo número de electrones de valencia y se puede decir que presentan las mismas propiedades químicas.
a) Incorrecta
El arreglo vertical de elementos es el grupo, no el periodo.
b) Incorrecta
En el arreglo vertical (grupo) de los elementos, se manifiestan propiedades químicas similares.
c) Incorrecta
En un grupo, los elementos presentan orbitales similares en el nivel de valencia (ejemplo: IA: ...ns1), pero las propiedades químicas son similares, mas no las nucleares.
d) Correcta
En un grupo, los elementos presentan propiedades químicas similares.
Rpta. : "D"
PREGUNTA 2 :
Los fertilizantes y plaguicidas son sustancias que causan daños en diferentes medios. Por ello, se debe establecer medidas para establecer un control del mismo. Seleccione el valor de verdad (V o F) de las siguientes proposiciones.
I) Los fertilizantes al llegar a los lagos producen la eutrofización.
II) Los pesticidas contaminan el aire, siendo muchos de tipo persistentes.
III) La lluvia ácida daña a la vegetación y puede formar desertificación.
A) VFF
B) VVV
C) FVF
D) FVV
E) FFV
RESOLUCIÓN :
I. VERDADERO
El control biológico reduce la población de plagas por medio de la introducción de predadores, parásitos u organismos patógenos, por lo cual se elimina el uso de insecticidas.
II. VERDADERO
Los pesticidas como el DDT son considerados como contaminantes orgánicos persistentes (COP), contaminando el aire, el agua y los suelos.
III. VERDADERO
La lluvia ácida puede producir daño a la vegetación, así como a las construcciones (corrosión), produciendo incluso desertificación de los suelos.
Rpta. : "B"
PREGUNTA 3 :
Los elementos y los compuestos son sustancias puras. Mientras que los primeros poseen en su composición átomos de un solo elemento, los compuestos están formados por la combinación de dos o más elementos. Se sabe que en el aire hay, principalmente, oxígeno y nitrógeno, y, en menor proporción, dióxido de carbono, metano y gases raros. Luego, es válido afirmar que el aire constituye una
I) mezcla de compuestos únicamente.
II) solución en estado gaseoso.
III) mezcla de elementos únicamente.
IV) mezcla de elementos y compuestos.
A) I y II
B) II y III
C) III y IV
D) II y IV
E) I y IV
RESOLUCIÓN :
El aire es una mezcla gaseosa homogénea, es decir, presenta una sola fase.
A las mezclas homogéneas también se les conoce como soluciones.
La composición del aire en proporciones ligeramente variables es:
– 78% nitrógeno (N₂) sustancia pura (1 elemento)
– 21% oxígeno (O₂) sustancia pura (1 elemento)
– 0,9% argón (Ar) sustancia pura (1 elemento)
– 0,04% dióxido de carbono (CO2) sustancia compuesta (2 elementos)
– Otros como el metano (CH4) sustancia compuesta (2 elementos)
Son correctas las proposiciones II y IV.
Es una solución (mezcla homogénea) en estado gaseoso de elementos como el N2, O2, Ar y compuestos como CO2 y CH4
Rpta. : "D"
PREGUNTA 4 :
Muchos elementos pesados como, plomo, arsénico, cadmio, mercurio, entre otros, afectan a la agricultura y con ello a los alimentos, contaminándolos. Con respecto al suelo y su contaminación, seleccione el valor de verdad (V o F) de las siguientes proposiciones.
I) Su contaminación también se da por materia orgánica y microorganismos.
II) Los insecticidas y agroquímicos producen contaminación al ambiente.
III) Un derrame de petróleo realiza un impacto en los ecosistemas presentes en ella.
A) VFF
B) VVV
C) FVF
D) FVV
E) FFV
RESOLUCIÓN :
I. VERDADERO
La materia orgánica en descomposición contenido en los residuos sólidos, así como también los microorganismos son parte de la contaminación de los suelos por el daño que origina a los ecosistemas.
II. VERDADERO
Los insecticidas y agroquímicos pueden ser cancerígenos al ser bioacumulado por los organismos, producen daños al metabolismo y a los ecosistemas.
III. VERDADERO
El derrame de petróleo contamina a los suelos, dañando a los ecosistemas evitando la relación entre la parte biótica y abiótica.
Rpta. : "B"
PREGUNTA 5 :
Si se transita por la avenida Abancay del centro de Lima se puede observar un alto nivel de contaminación ambiental, no solo por la presencia multitudinaria de personas y la basura arrojada a la calle, sino también por la presencia de gran cantidad de vehículos que emiten gases, entre los que se puede mencionar el CO2, el cual retiene la radiación infrarroja. De otro lado, en los domicilios se contamina el agua usando detergentes de diversos tipos. Respecto de la contaminación, establezca el valor de verdad (V o F) de las siguientes proposiciones.
I) Un contaminante es toda sustancia o especie que se encuentra en exceso en un lugar determinado.
II) El efecto invernadero evita que la totalidad de la energía irradiada por la superficie terrestre escape al espacio y se pierda.
III) La capa de ozono se encuentra ubicada en la estratosfera y es benéfica.
IV) Los detergentes modernos contienen polifosfatos y evitan la eutrofización.
A) VFVF
B) VVVF
C) FFVF
D) VVFV
E) FFFV
RESOLUCIÓN :
I. Verdadero
Un contaminante es una sustancia (S) que está en exceso en un lugar y que afecta a los seres vivos y el medio ambiente.
II. Verdadero
En el efecto invernadero, el calor del sol que llega a la Tierra evita que la totalidad de la energía infrarroja irradiada por la superficie terrestre escape al espacio y se pierda.
III. Verdadero
La capa de ozono (O3) se encuentra en la estratósfera e impide el paso total de los rayos ultravioleta (UV), que son nocivos ya que producen cáncer a la piel.
IV. Falso
La eutrofización es el crecimiento acelerado de hongos y plantas en la superficie de un lago, que se da por acción de nutrientes (nitrato y fosfato) y que derivan de los detergentes.
Rpta. : "B"
PREGUNTA 6 :
La fabricación del vidrio se inventó en Egipto hace aproximadamente 5 mil años al calentar una mezcla de arena, cenizas vegetales y piedra caliza. En 1674, G. Ravenscroft sustituyó la piedra caliza por óxido de plomo y obtuvo un vidrio más pesado y también más blando que podía pulirse. Fue hasta el siglo XIX, cuando se conoció la composición química de este material: dióxido de silicio, carbonato de sodio y carbonato de calcio. El color se debe a la presencia de óxidos metálicos en pequeñas cantidades; por ejemplo, de hierro para el color café, de cobalto para el azul, de oro para el rojo.
Determine el valor de verdad (V o F) de los siguientes enunciados:
I) el carbonato de sodio tiene por fórmula Na2CO3.
II) el vidrio, arena y cenizas vegetales son compuestos.
III) el compuesto dióxido de silicio es óxido básico.
IV) la piedra caliza es la mezcla de CaCO3 y CaO.
A) VFVV
B) VFVF
C) FFFV
D) FVVF
E) VFFV
RESOLUCIÓN :
NOMENCLATURA INORGÁNICA
I. Verdadero:
El carbonato de sodio, que representa la unión electrostática del catión Na+ (monopositivo) con el oxoanión CO32– (dinegativo). Al cruzar los estados de oxidación obtenemos: Na2CO3
II. Falso:
Tanto el vidrio, la arena como las cenizas son mezclas no son compuestos. El vidrio contiene arena de sílice (SiO2), carbonato de sodio (Na2CO3) y caliza (CaCO3), la arena contiene sílice, con fragmentos de sales y hierro y las cenizas son una mezcla del producto de la combustión de algún material, compuesto por sustancias inorgánicas no combustibles, como diferentes sales minerales, CO2 etc.
III. Falso:
El dióxido de silicio, sería un óxido ácido o clásicamente un anhídrido. Tiene propiedades ácidas al reaccionar con los óxidos básicos. Algunos ácidos silícicos simples han sido identificados, pero únicamente en disoluciones acuosas sumamente diluidas.
IV. Verdadero:
La piedra caliza es considerada una roca sedimentaria compuesta mayoritariamente por carbonato de calcio (CaCO3), generalmente calcita, aunque frecuentemente presenta trazas de magnesita (MgCO3) y otros carbonatos. Sin embargo, como roca sedimentaria en su proceso de transformación se puede encontrar pequeñas trazas de CaO (óxido de calcio), el cual también se obtiene por calentamiento total o parcial de la caliza.
Rpta. : "E"
PREGUNTA 7 :
La mineralización del tejido conjuntivo genera la estructura ósea, cuya composición es básicamente, cristales de hidroxiapatita Ca10(PO4)6(OH)2. Respecto de este compuesto, marque la alternativa incorrecta.
Dato: P.A. Ca=40
A) La hidroxiapatita se considera una sal de tipo básica.
B) Para un mol de hidroxiapatita, hay 1,2×1024 de aniones totales.
C) En un mol de hidroxiapatita, hay 1,56×1025 átomos de oxígeno.
D) Por cada mol de hidroxiapatita, hay 0,4 kg de calcio.
E) Cinco mol de hidroxiapatita tienen 220 mol de átomos totales.
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 8 :
En el proceso metalúrgico de tostación, se produce gases de óxido de azufre (SOx). Bajo ciertas condiciones, esta sustancia liberada al ambiente puede reaccionar con el agua presente en la atmósfera formando el ácido sulfúrico. Este ácido acuoso, al precipitarse sobre los suelos, produce la lixiviación de iones, como el potasio (K+) acuoso. Respecto de lo señalado, determine el valor de verdad (V o F) de las siguientes proposiciones:
I. El gas producido en la tostación forma inicialmente una mezcla homogénea con el aire atmosférico.
II. Al reaccionar con agua, los SOx forman un ácido oxácido y esta mezcla puede precipitarse en forma acuosa.
III. La lixiviación de los iones de potasio implica su disolución desde la fase sólida.
A) VVV
B) VFF
C) FVF
D) FFV
E) VVF
RESOLUCIÓN :
METALURGÍA
respecto a los cambios que ocurren en cierto proceso metalurgico.
La tostación es un proceso aplicado a los minerales metálicos que contienen azufre, del cual se produce SOx (SO2 y SO3); formándose primero el SO2 y luego SO3.
SO2(g)+ O2(g)→ SO3(g)
I. Verdadero
SO2(g)+ (aire) → mezcla gaseosa es homogénea.
II. Verdadero
SO3(g)+ H2O(v) → H2SO4(ac)
Al precipitarse es llamada lluvia ácida.
III. Verdadero
La lixiviación, provocada por la lluvia ácida, disuelve al ion potasio K+ desde los minerales del suelo (fase sólida), y se forma una disolución acuosa que contiene K+, lo que causa una bata en la fertilidad del suelo.
Rpta. : "A"
PREGUNTA 9 :
Cuando se saca simultáneamente una botella de gaseosa de una congeladora (temperatura promedio igual a –18°C) y otra de la refrigeradora (temperatura promedio igual a 4°C), se observa que en la superficie de la primera se forma escarcha y en la segunda, pequeñas gotas de agua. Respecto de lo que sucede en la superficie de estas botellas, determine la alternativa correcta.
A) En la primera hay un cambio químico y en la segunda un cambio físico.
B) En ambas botellas se producen cambios estructurales del agua.
C) El cambio en la segunda botella se denomina condensación.
D) El cambio en la primera botella se denomina sublimación directa.
E) En las dos botellas se produce liberación de calor al entorno.
RESOLUCIÓN :
Es importante mencionar que el vapor de agua se halla en ambos sistemas, pero cuando el vapor entra en contacto con el recipiente que está a –18°C, el vapor pasa directamente a la fase sólida (produciéndose una sublimación inversa), mientras que el vapor que entra en contacto con el recipiente a 4°C, pasa a la fase líquida (produciéndose una condensación).
Rpta. : "C"
PREGUNTA 10 :
En Lima tenemos a SEDAPAL, una empresa del Estado que brinda servicios de agua potable, cumpliendo los estándares de calidad para beneficiar a la población. Con respecto al proceso de potabilización del agua de los ríos, seleccione la(s) proposición(es) correcta(s).
I) La sedimentación separa coloides de gran tamaño contenida en el río.
II) El Aℓ2(SO4)3.14H2O disminuye partículas sedimentables del agua.
III) El proceso de cloración disminuye la carga microbiológica.
A) Solo II
B) Solo I
C) I y III
D) II y III
E) I y II
RESOLUCIÓN :
I. INCORRECTO
La sedimentación separa partículas finas que son afectas por la gravedad. Los coloides no son afectados por la gravedad, por lo tanto, no pueden sedimentar.
II. CORRECTO
El Aℓ3(SO4)3.14H2O es usado para la coagulación y floculación de partículas que causan la turbidez del agua, es decir, los coloides.
III. CORRECTO
La cloración con sustancias como el Cℓ2(g) o la lejía (NaCℓO(ac)) disminuyen la carga bacteriana.
Rpta. : "D"
PREGUNTA 11 :
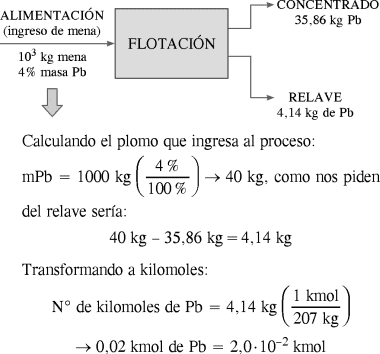
La flotación es un proceso metalúrgico que consiste en obtener concentrados a partir de minerales presentes en sus menas, además del relave que sigue conteniendo parte del metal. Se muestra un esquema de un proceso de flotación con información de su desarrollo.
Determine los kilomol de plomo que pasó al relave cuando finalizó el proceso de flotación.
Dato: P.A. Pb = 207g / moL
A) 4,0×10–3
B) 4,0×10–2
C) 2,0×10–3
D) 2,0×10–2
E) 2,0×10–4
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 12 :
Las reacciones químicas implican transformación de la materia. Cuando consumimos alimentos como el azúcar (sacarosa), nuestro organismo obtiene energía mediante el proceso llamado metabolismo. Un proceso inverso que necesita energía es la fotosíntesis. Lo expuesto se muestra en el siguiente esquema:
Al respecto, establezca el valor de verdad (V o F) de las siguientes proposiciones:
I. La sacarosa y el agua se clasifican como mezclas.
II. El dióxido de carbono y el agua son compuestos moleculares.
III. La combustión y la fotosíntesis son cambios químicos exotérmicos.
IV. La disolución de azúcar en agua corresponde a un cambio físico.
A) FFFV
B) VFFV
C) FVVV
D) VVFF
E) FVFV
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 13 :
Las reacciones de combustión son utilizadas por la industria para obtener energía en forma de calor. Los hidrocarburos, como el metano, son utilizados según lo muestra la ecuación química:
CH4(g)+O2(g)→ CO2(g)+H2O(v)
ΔH= – 890 kJ/mol
Al respecto, indique el valor de verdad (V o F) de las siguientes proposiciones:
I. Se produce 20 mol de agua, con un rendimiento de 50%, por el ingreso inicial de 3,2×102 gramos de metano.
II. En una reacción al 100% de rendimiento, si se hace reaccionar 0,32 gramos de oxígeno, se libera 4,45 kJ de energía.
III. Si 0,8 mol de metano reacciona con 12,8 gramos de oxígeno, el reactivo en exceso es el metano.
Datos: H=1, O=16, C=12
A) FVF
B) VVF
C) VVV
D) VFV
E) FVV
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 14 :
El pH de nuestra sangre varía entre 7,3 y 7,5. Mientras nos mantenemos con vida, nuestro pH sanguíneo varía muy poco, debido a la presencia de soluciones reguladoras en nuestro organismo. Una de estas soluciones es el par ácido carbónico y ion bicarbonato (HCO3–) que se produce, durante la respiración celular, al reaccionar el CO2 con el agua del plasma sanguíneo según
Respecto de estas reacciones o de sus componentes, marque el valor de verdad (V o F) de las siguientes proposiciones:
I. a) representa una reacción heterogénea.
II. En b), el ácido carbónico se disocia parcialmente en iones.
III. En a) y b), el carbono no cambia su estado de oxidación.
IV. La segunda ecuación representa una reacción en equilibrio.
A) FFVV
B) VVVF
C) FVFV
D) VVFF
E) VVVV
RESOLUCIÓN :
ÁCIDOS Y BASES
I. Verdadero
La primera reacción es heterogénea porque las sustancias están en diferentes fases.
II. Verdadero
En la segunda reacción, el H2CO3 se disocia parcialmente ya que es reversible el proceso.
III. Verdadero
En ambas reacciones químicas, el estado de oxidación del carbono es +4.
IV. Verdadero
La segunda reacción formará un equilibrio por ser reversible (doble sentido).
Rpta. : "E"
PREGUNTA 15 :
El oxígeno y el dióxido de carbono ingresan a los pulmones y, después, el oxígeno es transportado, principalmente, por la sangre hasta las células. Luego de la respiración celular, el dióxido de carbono es transportado por el eritrocito, pero parte de esta sustancia se combina con el agua y por acción de la anhidrasa carbónica, forma el ion bicarbonato. Con respecto al enunciado anterior, determine el valor de verdad (V o F) de las siguientes proposiciones:
I. El O2 y el CO2 son compuestos moleculares que ingresan a los pulmones en fase gaseosa.
II. El CO2 producido en la respiración celular es transportado en forma de mezcla gaseosa.
III. El oxoanión (HCO3)–2 es transportado en forma iónica por la sangre.
A) VFF
B) FFF
C) VFV
D) FVF
E) FFV
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 16 :
Experimentalmente, y bajo condiciones muy especiales, se comprueba que una de las estructuras más representativas para el dióxido de dinitrógeno corresponde a una molécula lineal en la que todos los átomos retienen sus respectivos pares solitarios. Identifique la afirmación que corresponde a la representación de Lewis.
Datos: 7N y 8O
A) La molécula lineal presenta cuatro pares de electrones solitarios.
B) Los enlaces covalentes heteronucleares del N2O2 son no polares.
C) Los dos átomos de nitrógeno están unidos por un triple enlace.
D) Los dos átomos de nitrógeno forman un enlace covalente simple.
E) La molécula lineal presenta 3 pares de electrones libres.
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 17 :
La lluvia ácida es una forma de contaminación ambiental debido a la emisión de ciertas sustancias a la atmósfera; estos gases en conjunto con el agua permiten la formación de este tipo de contaminación. Con respecto a la lluvia ácida, seleccione la(s) proposición(es) correcta(s).
I) Los gases emitidos que generan la lluvia ácida son los NOx y el SO2.
II) Su precipitación aumenta el pH de los lagos dañando ecosistemas.
III) Puede causar procesos de desertificación por el impacto en la vegetación.
A) II y III
B) Solo II
C) I y II
D) I y III
E) Solo I
RESOLUCIÓN :
I. CORRECTO
Los gases emitidos de NOx y SO2 reaccionan con el agua de la atmósfera para producir los ácidos respectivos:
NOx + H2O → HNO3
SOx + H2O → H2SO4
II. INCORRECTO
La precipitación de la lluvia ácida incrementa la concentración de iones hidrógeno (H+), disminuyendo el pH de los lagos, causando daños en los ecosistemas.
III. CORRECTO
La lluvia ácida al impactar en los suelos puede dañar a la vegetación. Produciendo a largo plazo un proceso de desertificación.
Rpta. : "D"
PREGUNTA 18 :
La fosfina (PH3) se considera un hidruro no metálico. Es un compuesto formado por la unión de un no metal con el hidrógeno. Este hidruro especial es un gas tóxico y una forma de obtenerlo es a partir de la siguiente reacción:
P4(s)+3NaOH(ac)+3H2O(ℓ)→ 3NaH2PO2+PH3(g)
Con respecto a lo mencionado seleccione la alternativa correcta.
A) La fosfina tiene enlaces covalentes y se forma a partir de un compuesto homonuclear (P4).
B) Conjuntamente a la fosfina, se forma un producto iónico (sal oxisal de tipo básica).
C) Según Lewis, el hidruro especial carece, por completo, de electrones no enlazantes.
D) La fosfina es una base débil pues acepta un protón del agua en un medio acuoso.
E) Un mol de fosfina contiene un átomo de un no metal de tipo nitrogenoide (V A).
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 19 :
En el cuerpo humano, el metabolismo de la glucosa produce CO2 , que es eliminado de los pulmones como un gas de acuerdo con la siguiente reacción:
Determine la secuencia correcta del valor de verdad (V o F) en relación con los siguientes enunciados.
I) Se trata de una reacción redox.
II) Es una reacción de combustión completa.
III) Se trata de una reacción exotérmica.
A) VFV
B) FVV
C) VVF
D) VFF
E) VVV
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 20 :
El agua potable contiene carbonatos, bicarbonatos, iones calcio, iones magnesio, etc., por lo cual se la conoce como agua dura. Esta ocasiona la formación del sarro en las tuberías de agua o en las paredes del recipiente donde se hierve el agua. Para removerlo, se utiliza ácido clorhídrico según la reacción
CaCO3(s)+HCI(ac)→ CaCl2(ac) +H2O(ℓ)+CO2(g)
Una forma de comprobar que realmente se está removiendo el sarro es reconocer el desprendimiento de CO2(g), que, al reaccionar con el hidróxido de calcio, forma nuevamente carbonato de calcio.
Respecto de lo expresado, determine el valor de verdad (V o F) de las siguientes proposiciones:
I. Si el agua dura contiene sales de carbonato de magnesio, al reaccionar con el ácido clorhídrico, produce la sal haloidea cloruro de magnesio.
II. Para reconocer el CO2(g), la ecuación química es la siguiente:
CO2(g)+Ca(OH)2(ac)→ CaCO3(s)+H2O(ℓ)
III. Las causantes del sarro son sales oxisales, donde la carga catiónica se debe a los metales del grupo IIA.
IV. La sumatoria de coeficientes en la ecuación que representa la remoción del sarro es cinco.
A) VVFV
B) VFVV
C) FVVF
D) VVFF
E) VVVF
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 21 :
En el siguiente esquema, se muestra un proceso de electrólisis en el que circula una carga equivalente a 20 Faraday. En relación a lo señalado, determine el valor de verdad (V o F) de las siguientes proposiciones:
Datos: P. atómico O =16, H=1
I. En el catodo, se libera 5 mol de O2 gaseoso.
II. En el ánodo, se libera 6×1024 moléculas de H2.
III. Se libera 20 equivalentes de H2 y O2, respectivamente.
IV. La masa, en gramos, de oxígeno e hidrógeno liberada es 160 y 20, respectivamente.
A) FVFV
B) VVFF
C) FFVV
D) VFFV
E) FFVF
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 22 :
Estructuralmente el ácido oxálico es el ácido etanodioico, contenido en las hojas verdes como la espinaca. Respecto de este ácido, determine el valor de verdad (V o F) de las siguientes proposiciones:
I. El ácido oxálico es un ácido débil y puede formar sales.
II. El ácido oxálico se puede formar por oxidación del etanol.
III. La fórmula global del oxalato de calcio es CaC2O4.
A) FVF
B) FVV
C) VFF
D) VVF
E) VFV
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 23 :
Cuando la concentración de NaCl en el suero fisiológico es 0,154M, el valor que corresponde en unidades de porcentaje peso/volumen es
Dato masas atómicas: Na=23 ; Cl=35,5
A) 0,999
B) 9,0
C) 0,009
D) 0,0009
E) 0,9
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 24 :
Las soluciones iónicas permiten obtener concentraciones de diferentes iones para ser utilizados en experimentos de simulación fisiológica. Considere el siguiente gráfico y determine el valor de verdad (V o F) de las siguientes proposiciones respecto de la solución salina resultante:
Datos: Masa molar: NaCl=58,5 y KCl=74
I. La solución salina contiene 580 mEq de aniones Cl–.
II. En un litro de solución original de cloruro de sodio está presente 140 mEq de Na+.
III. En la solución salina, están presentes 200 mEq de iones K+.
A) VVF
B) FVV
C) FVF
D) VFF
E) FFV
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 25 :
La descomposición
ocurre mediante una reacción sencilla a 325ºC. ¿Cuál será la concentración final, en mol/L, del N2O5 a los 200 segundos, luego de haber iniciado la reacción con una concentración inicial del N2O5(g) de 6,50×10–4mol/L y cuando el valor de k es 5×10–4s–1?
A) 6,50×10–5
B) 2,50×10–7
C) 6,25×10–4
D) 4,45×10–4
E) 5,85×10–4
RESOLUCIÓN :
Rpta. : "E"
PREGUNTA 26 :
Se hace circular una corriente de 60 A durante 3,86×10–3 segundos, a través de una solución que contiene cloruro de magnesio fundido (ecuación química:
MgCℓ2(ℓ) → Mg(ℓ) + Cℓ2(g)
La masa de magnesio en gramos y el volumen de cloro, a condiciones normales, obteniendo en mililitros, respectivamente, es:
Datos: Peso atómico Mg = 24; cloro = 35,5
A) 57,6 – 2,68×104
B) 14,4 – 2,68×104
C) 28,8 – 2,68×104
D) 28,8 – 5,36×103
E) 14,4 – 5,36×103
RESOLUCIÓN :
Rpta. : "C"
PREGUNTA 27 :
El cloruro de sodio (NaCl) es un sólido conocido como sal, mineral muy abundante en nuestro planeta. Está presente en el agua de mar y en las formaciones rocosas de tipo subterráneo. Sus iones sodio y cloruro están ordenados en disposiciones bien definidas y son los componentes de la celda unitaria de NaCℓ.
Con respecto a la información ofrecida, determine el valor de verdad (V o F) de las siguientes proposiciones:
I) La sal cloruro de sodio (NaCℓ) es un compuesto con un alto punto de fusión y es considerado un sólido de tipo amorfo.
II) El ion sodio, presente en la estructura sólida, tiene menor tamaño que su átomo neutro debido a su condición de catión.
III) Los iones cloruro tienen gran volumen en la celda unitaria y se pueden formar a partir de la reducción del cloro atómico.
A) FVV
B) VFF
C) FVF
D) VFV
E) FFV
RESOLUCIÓN :
Rpta. : "A"
PREGUNTA 28 :
El fenol es un sólido cristalino incoloro y brillante, muy soluble en agua, alcohol y éter. En la naturaleza se lo encuentra en la madera y se lo prepara artificialmente para ser usado como desinfectante. Identifique el nombre de la siguiente estructura.
A) p-hidroxitolueno
B) m-metilfenol
C) 4-metilciclohexanol
D) 4-metilfenol
E) 3-metilfenol
RESOLUCIÓN :
Rpta. : "D"
PREGUNTA 29 :
El etanol, conocido como alcohol etílico, puede presentarse como una mezcla con un grado alcohólico de 96° y es el componente principal de bebidas destiladas, como el pisco peruano. También es utilizado como desinfectante, pues produce la ruptura de la pared bacteriana, pero entonces su grado alcohólico es 70° y se conoce como alcohol medicinal. Respecto de lo señalado, determine el valor de verdad (V o F) de los siguientes enunciados:
I. Alcohol etílico, pisco peruano y alcohol medicinal son mezclas homogéneas.
II. El alcohol etílico a temperatura ambiente se presenta en fase gas y es soluble en agua.
III. Las moléculas de etanol presentan, predominantemente, fuerzas intermoleculares de tipo puente de hidrógeno.
IV. El etanol es una molécula polar con dos pares de electrones libres.
A) VFVF
B) FFVV
C) FVFV
D) VVFV
E) FFVF
RESOLUCIÓN :
Rpta. : "B"
PREGUNTA 30 :
El aspartame es una sustancia que se encuentra en bebidas y refrescos dietéticos (no calóricos). Su estructura molecular contiene restos de ácido aspártico, fenilalanina y metanol. Respecto de su estructura y sus propiedades, establezca la relación correcta.
I) Tiene propiedades ácidas.
II) Es soluble en agua.
Tiene e– 𝛑 deslocalizados.
a. Anillo aromático
b. Grupo carboxilo
c. Forma puentes de hidrógeno
A) Ib, IIa, IIIc
B) Ia, IIb, IIIc
C) Ic, IIa, IIIb
D) Ib, IIc, IIIa
E) Ia, IIc, IIIb
RESOLUCIÓN :
Es importante recordar que las propiedades de una sustancia están directamente relacionadas con los grupos funcionales que presenta, por lo que, en el aspartame, un edulcorante usado en la industria
En el aspartame se observa que el grupo carboxilo exhibe propiedades ácidas, en el grupo aromático los electrones se encuentran deslocalizados. Por otro lado, los pares libres del nitrógeno y oxigeno forman enlace puente de hidrogeno con el agua y por ello su solubilidad.
Rpta. : "D"
PREGUNTA 31 :
El fenómeno de smog fotoquímico es producido por gases contaminantes, ellos son oxidantes, por ejemplo, ozono (O3), emitidos por diversos procesos y su posterior interacción en la atmósfera. Al respecto, seleccione la secuencia correcta de verdad (V o F) respectivamente.
I) Este contaminante secundario es formado como producto de la interacción de los gases como el NOx y la luz solar.
II) Las sustancias contenidas en el smog fotoquímico, son el nitrato de peroxiacilo (PAN), ozono troposférico (O3) y las partículas suspendidas de sílice.
III) Los compuestos orgánicos volátiles (COV´s), pueden afectar la salud de las personas produciendo daños a nivel celular.
A) VVV
B) FFV
C) VVF
D) VFV
E) VFF
RESOLUCIÓN :
I. VERDADERO
el smog fotoquímico es un fenómeno formado como producto de la interacción de los gases como el NOx y la luz solar.
II. FALSO
las sustancias contenidas en el smog fotoquímico son por ejemplo el nitrato de peroxiacilo (PAN), ozono troposférico (O3) así como también los compuestos orgánicos volátiles (COV´s), partículas de sílice no son parte del smog fotoquímico, pero si son dañinas para el sistema respiratorio.
III. VERDADERO
los compuestos orgánicos volátiles (COV´s), son sustancias como el benceno y estas pueden afectar la salud de las personas produciendo daños a nivel celular como, por ejemplo, daños hepáticos y renales.
Rpta. : "D"