QUÍMICA PRE SAN MARCOS SEMANA 10 SOLUCIONARIO PROBLEMAS RESUELTOS PDF
ESTADO SÓLIDO:
☛ Sólido cristalino y sólido amorfo, sublimación.
☛ Solubilidad y los sistemas dispersos.
☛ Tipos de dispersiones.
☛ Soluciones y unidades de concentración:
☛ Unidades físicas (%W/W, %W/V, %V/V).
☛ Unidades químicas de concentración (M y N).
☛ Ácidos, bases y sales:
☛ Definiciones, reacciones de los ácidos y reacciones de las bases,
neutralización ácido-base
☛ Concepto de pH.
PREGUNTA 1 :
El estado sólido se caracteriza por tener un volumen definido y una alta densidad debido a que las partículas que lo constituyen se encuentran muy cerca entre ellas. Con respecto al estado sólido, indique la alternativa INCORRECTA.
A) Las fuerzas de repulsión son menores que las de cohesión.
B) La madera, el vidrio y el caucho son sólidos amorfos.
C) El hielo seco (CO2(s)) es un sólido cristalino molecular.
D) Los sólidos iónicos conducen la electricidad a 25°C.
Rpta. : "D"
PREGUNTA 2 :
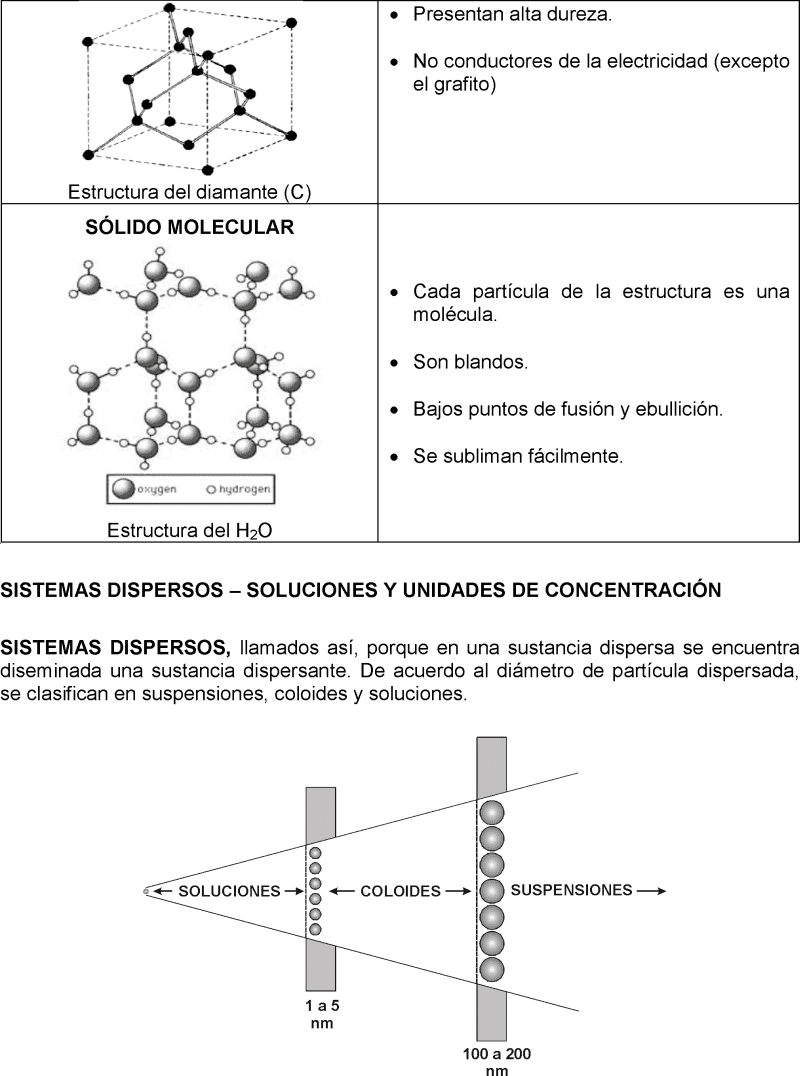
Los sistemas dispersos son mezclas en la que una o más sustancias se encuentran diseminadas en un medio y se clasifican según el tamaño de las partículas dispersas en soluciones, coloides y suspensiones.
Al respecto, indique el valor de verdad (V o F) de las siguientes proposiciones.
I. Las partículas dispersas de un coloide son de menor tamaño que las de una suspensión.
II. Las soluciones y los coloides son sistemas dispersos homogéneos debido a que presentan una fase.
III. El aire es una solución, el humo es un coloide y el jugo de frutas es una suspensión.
A) FVF
B) VFV
C) VVV
D) VFF
Rpta. : "B"
PREGUNTA 3 :
El gasohol E10 es una solución formada por 90% en volumen de gasolina y 10% en volumen de etanol y se puede emplear como combustible en la mayoría de vehículos modernos. Si se emplea 4 L de gasohol E10, determine el porcentaje masa / volumen de etanol en dicha solución.
Dato: Densidad etanol = 0,78 g/mL
A) 3,9
B) 9,0
C) 7,8
D) 4,5
Rpta. : "C"
PREGUNTA 4 :
Las soluciones de soda cáustica (NaOH) se emplean como agente de limpieza de equipos de acero inoxidable. Si se tiene 450g de dicha solución al 48% en masa y una densidad de 1,5 g/mL, determine su concentración expresada en ppm.
A) 7,2×10–1
B) 3,6×105
C) 7,2×105
D) 3,6×10–1
Rpta. : "C"
PREGUNTA 5 :
La dilución es una operación física que consiste en agregar una mayor cantidad de solvente a una solución, con la finalidad de disminuir su concentración. En una práctica de laboratorio un estudiante adiciona 400 mL de agua a 800 mL de una solución de CaCℓ2 3,0 M, determine la normalidad de la solución resultante.
A) 1,5
B) 2,0
C) 3,0
D) 4,0
Rpta. : "D"
PREGUNTA 6 :
El ácido nítrico (HNO3) es altamente corrosivo, provoca quemaduras al entrar en contacto con los ojos o la piel y debido a su peligrosidad se disuelve con mucho cuidado en agua evitando salpicaduras. Determine el volumen, en litros, de HNO3(ac) 1,0 M que se requiere mezclar con 2L de HNO3(ac) 12,0 M, para obtener una solución de HNO3(ac) 6,0 M (considere volúmenes aditivos).
A) 1,2
B) 3,6
C) 2,4
D) 4,8
Rpta. : "C"
PREGUNTA 7 :
En un ensayo de laboratorio un analista toma una muestra de 20 mL de una solución de HCℓ 1 N y lo vierte en un matraz, luego le adiciona 30 mL de una solución de KOH 1,5 N, produciéndose una reacción de neutralización. Al respecto, indique el valor de verdad (V o F) de las siguientes proposiciones.
I. Se tiene en el matraz inicialmente 2×10–2 eq del ácido.
II. Se añade al matraz 4,5×10–1 eq del KOH.
III. Al culminar la reacción la solución resultante tiene un pH mayor a 7.
A) VFV
B) FVF
C) FFV
D) VVF
Rpta. : "A"
PREGUNTA 8 :
En la naturaleza encontramos una gran cantidad de sólidos con diversas aplicaciones, tales como el cuarzo (SiO2) usado en la fabricación del vidrio, calcita (CaCO3) empleada en la producción del cemento y el hielo seco (CO2(s)) utilizado para mantener los alimentos a bajas temperaturas.
Al respecto, indique la alternativa correcta.
A) El vidrio es un sólido cristalino de red covalente.
B) La calcita conduce la electricidad a 25°C.
C) El cuarzo presenta una baja dureza.
D) El hielo seco tiene baja temperatura de fusión.
Rpta. : "D"
PREGUNTA 9 :
El agua regia es una solución que contiene HNO3 y HCℓ, dicha mezcla es altamente corrosiva y es capaz de reaccionar con el oro y el platino. Si se tiene 500 mL de agua regia cuya densidad es 1,25 g/mL, la cual contiene HNO3 al 25 % en volumen, determine el porcentaje en masa del ácido nítrico en dicha solución.
Dato: Densidad: HNO3= 1,50 g/mL
A) 15,0
B) 30,0
C) 45,0
D) 7,5
Rpta. : "B"
PREGUNTA 10 :
Las soluciones de potasa cáustica (KOH) se emplean en la producción de fertilizantes y detergentes. Si se disuelve 6,72 g de KOH en cantidad suficiente de agua para formar 200 mL de solución, determine la molaridad y normalidad de dicha solución, respectivamente.
Dato:M(g/mol) : KOH = 56
A) 0,6 y 1,2
B) 1,2 y 0,6
C) 1,2 y 1,2
D) 0,6 y 0,6
Rpta. : "D"
PREGUNTA 11 :
Las reacciones de neutralización son utilizadas en el tratamiento de aguas residuales, ya que se utilizan para adecuar el pH a valores permitidos. Si se tiene agua residual que contiene 50 mL de H2SO4 0,1 M y se neutraliza con una solución de NaOH 0,2 M, determine el volumen, en L, necesarios de la solución básica, para que el pH de la solución final sea igual a 7,0.
A) 5,0×10–1
B) 2,5×10–2
C) 2,5×10–1
D) 5,0×10–2
Rpta. : "D"