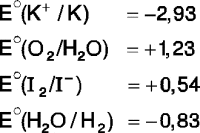SIMULACRO UNI 2026 TERCERA PRUEBA DE INGRESO SOLUCIONARIO UNIVERSIDAD DE INGENIERÍA PDF
CLAVES – RESPUESTAS :
1)A 2)A 3)A 4)D 5)A 6)B 7)E 8)E 9)C 10)A 11)D 12)A 13)A 14)B 15)E 16)D 17)D 18)E 19)A 20)A 21)E 22)C 23)C 24)E 25)D 26)E 27)A 28)C 29)D 30)A 31)A 32)B 33)C 34)D 35)B 36)B 37)C 38)C 39)A 40)A
FÍSICA
PREGUNTA 1 :
Un rifle ubicado sobre el eje X dispara una bala con una rapidez de 457m/s. Un blanco pequeño se ubica sobre el eje X a 45,7m del origen de coordenadas. Calcule aproximadamente, en metros, la altura h a la que debe elevarse el rifle por encima del eje X, para que pueda dar en el blanco. Considere que el rifle siempre dispara horizontalmente.
( g=9,81m/s²)
A) 0,01
B) 0,02
C) 0,03
D) 0,04
E) 0,05
PREGUNTA 2 :
Un cuerpo se lanza hacia arriba desde una altura de 20m y alcanza una altura máxima (desde el suelo) de 30m en un tiempo t. Si t' es el tiempo que demora el cuerpo en caer al suelo desde la altura máxima, calcule t'/t. ( g=9,81 m/s²).
A) 1
B) √2
C) √3
D) 2
E) √5
PREGUNTA 3 :
La figura muestra un cuadrado ABCD de lado 1u. Si las curvas son arcos de circunferencia con centros en B y D, exprese el vector →c en términos de →a y →b
PREGUNTA 4 :
Se ha determinado que la magnitud F de una fuerza que actúa sobre un satélite que orbita la Tierra depende de la rapidez v del satélite, de la distancia media del satélite al centro de la Tierra R y de la masa m del satélite según la relación
Siendo K una constante adimensional, determine α+β+γ.
A) – 2
B) –1
C) 0
D) 1
E) 2
PREGUNTA 5 :
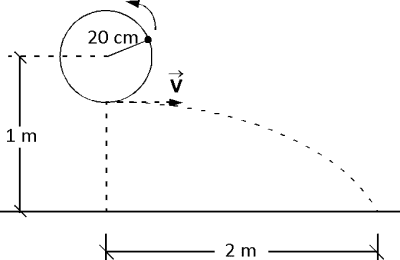
Un cuerpo de 200 g de masa gira en un plano vertical atado a una cuerda tensa de 20 cm de longitud. El eje del plano de giro se ubica a una altura de un metro del suelo. Cuando el cuerpo pasa por su punto más bajo la cuerda se rompe y el cuerpo cae a una distancia horizontal de 2 m como se muestra en la figura. Calcule la tensión de la cuerda (en N) en el momento que se rompe. ( g=9,81 m/s²)
A) 3,31
B) 6,62
C) 13,25
D) 26,49
E) 52,98
PREGUNTA 6 :
La hélice de un ventilador gira a 960 RPM. Después de desconectarlo, desacelera uniformemente demorando 16s hasta detenerse. Calcule el número de vueltas que realiza la hélice en la desaceleración.
A) 32
B) 64
C) 128
D) 256
E) 512
PREGUNTA 7 :
Una cuerda tensa de 1,5 m de longitud forma una onda estacionaria con 3 nodos entre sus extremos. Halle la longitud de onda de la onda estacionaria, en metros.
A) 1/4
B) 1/2
C) 3/4
D) 1
E) 5/4
PREGUNTA 8 :
Calcule aproximadamente la cantidad de calor, en kJ, que se desprende cuando 100g de vapor de agua a 150ºC se enfrían hasta convertirlo en 100g de hielo a 0ºC.
Calor específico de vapor de agua=2,01 kJ/kgK
Calor latente de vaporización del agua=2257 kJ/kg
Calor específico del agua líquida=4,18 kJ/kgK
Calor latente de fusión del agua=333,5 kJ/kg
A) 305
B) 311
C) 327
D) 332
E) 353
PREGUNTA 9 :
Un protón tiene una energía cinética E y sigue una trayectoria circular en un campo magnético de magnitud B. Encuentre el radio de la trayectoria.
m: masa del protón ;
q: carga eléctrica del protón.
PREGUNTA 10 :
Un condensador almacena 5 nJ de energía cuando se le aplica una diferencia de potencial V. Si se conectan en serie 5 condensadores idénticos al anterior y se les aplica en los extremos la misma diferencia de potencial V. Calcule (en nJ) la energía total que se almacena en el circuito.
A) 1
B) 2
C) 3
D) 4
E) 5
PREGUNTA 11 :
Una esfera de 200 cm³ de volumen que tiene una densidad igual a 0,8 g/cm³, está sumergida en un tanque lleno de agua. Si la esfera se suelta del fondo del tanque, calcule aproximadamente el tiempo (en s) que demora en elevarse 5 m dentro del agua.
No considere las fuerzas de fricción.
(g=9,81 m/s²).
A) 2,02
B) 3,02
C) 4,02
D) 5,02
E) 6,02
PREGUNTA 12 :
Una cuerda se fija por ambos extremos haciéndola vibrar bajo una tensión de 180 N generándose ondas estacionarias. Dos armónicos consecutivos tienen frecuencias de 45 Hz y de 37,5 Hz. Si la densidad lineal de masa de la cuerda es igual a 0,2 kg/m, calcule la longitud de la cuerda (en m).
A) 1
B) 2
C) 3
D) 4
E) 5
PREGUNTA 13 :
Se tiene un sistema formado por tres esferas pequeñas de igual masa (m=10g). En el instante t=0, se encuentran sobre una superficie horizontal lisa en las posiciones que se muestran en la figura. Si los choques son frontales y completamente inelásticos, determine la cantidad de movimiento del sistema (en g.cm/s) en el instante t=3s.
A) 9
B) 10
C) 20
D) 25
E) 30
PREGUNTA 14 :
Dos satélites idénticos S1 y S2 orbitan circularmente alrededor de un mismo planeta. El primero tiene un periodo de 512 horas y el segundo de 343 horas Calcule la relación de los radios de sus órbitas R1/R2
A) 16/15
B) 8/7
C) 41/35
D) 56/42
E) 64/49
PREGUNTA 15 :
Sobre una superficie metálica con función de trabajo igual a 3×10–19 J, incide una onda electromagnética. Calcule aproximadamente la máxima longitud de onda (en nm), que debe de tener la onda electromagnética para que se observe el efecto fotoeléctrico.
h=6,626×10–34 J · s
c =3×108 m/s
nm= 10–9 m
A) 321,2
B) 432,6
C) 662,6
D) 721,6
E) 932,8
PREGUNTA 16 :
El campo eléctrico máximo de una onda electromagnética es de 1,8 V/m. Calcule el campo magnético máximo (en nT).
c =3×108m/s; nT =10–96 T
A) 1
B) 2
C) 3
D) 6
E) 8
PREGUNTA 17 :
En el circuito mostrado la potencia total disipada es de 75 W, calcula la resistencia R (en Ω).
A) 1
B) 2
C) 3
D) 4
E) 5
PREGUNTA 18 :
En un ciclo de Carnot de un gas ideal ( γ=5/3) , se tiene que durante la expansión isotérmica el volumen se duplica y en la expansión adiabática el volumen aumenta en un 25%. Calcule la relación entre la máxima y mínima temperatura en este ciclo
A) (1/4)2/3
B) (3/4)2/3
C) (5/4)2/3
D) (7/4)2/3
E) (9/4)2/3
PREGUNTA 19 :
Halle aproximadamente la altura h sobre la superficie de la Tierra donde la aceleración de la gravedad es 1 m/s². El radio de la Tierra es R. ( g=9,81 m/s²).
A) 2,1R
B) 4,4R
C) 6,2R
D) 8,7R
E) 12,1R
PREGUNTA 20 :
Una persona tiene una altura H desde los ojos hasta el suelo y observa un espejo adherido a una pared que se encuentra a una distancia d, como se observa en el dibujo. Si el espejo se encuentra a una altura h del suelo, la distancia x más cercana a la pared a la que se puede ubicar un objeto para que la persona lo vea reflejado en el espejo es:
QUÍMICA
PREGUNTA 21 :
Indique el grupo y periodo de la tabla periódica, respectivamente, correspondiente a un elemento químico cuya configuración electrónica termina en
A) IA ; 4
B) IIIA ; 3
C) VA ; 4
D) VIIIB ; 3
E) IB ; 4
PREGUNTA 22 :
En los siguientes oxianiones, indique el que está correctamente nombrado.
PREGUNTA 23 :
Respecto al recurso agua, ¿cuáles de las siguientes proposiciones son correctas?
I) El agua nunca se encuentra pura en la naturaleza, debido a la facultad que tiene para disolver o dispersar diferentes sustancias.
II) El agua de lluvia recolectada, en la azotea de una vivienda, en un recipiente esterilizado, es agua pura.
III) La contaminación de las aguas con materia orgánica biodegradable disminuye la concentración de oxígeno disuelto.
A) solo I
B) solo II
C) solo III
D) I y III
E) I, II y III
PREGUNTA 24 :
Señale la alternativa que presenta la secuencia correcta, después de determinar si la proposición es verdadera (V) o falsa (F):
I) El número máximo de orbitales atómicos correspondientes al tercer nivel de energía es nueve.
II) Un orbital atómico tipo p presenta forma tetralobular.
III) El orbital atómico 7pz presenta mayor tamaño que el orbital atómico 6pz
A) VFV
B) VFF
C) FVV
D) VVV
E) FFF
PREGUNTA 25 :
Una de las preocupaciones a nivel mundial es el calentamiento global originado por las actividades del hombre.
Al respecto, señale la alternativa que presenta la secuencia correcta después de determinar si las proposiciones son verdaderas (V) o falsas (F).
I) El calentamiento global es consecuencia del aumento de la temperatura en la atmósfera terrestre.
II) El cambio climático que ocurre en la Tierra está relacionado principalmente al impacto de los gases de efecto invernadero.
III) El término efecto invernadero se refiere a la retención del calor en la atmósfera por parte de una capa de gases en la atmósfera, como por ejemplo el dióxido de carbono, el vapor de agua y metano.
A) VVV
B) VFV
C) VFF
D) FFV
E) FFF
PREGUNTA 27 :
La corrosión de un metal es un proceso espontáneo a temperatura ambiente.
Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I) La corrosión implica un proceso de oxidación reducción.
II) En algunos casos, la corrosión del metal forma una capa protectora que disminuye el proceso de corrosión.
III) El daño estructural por efectos de la corrosión tiene una alta repercusión económica.
A) solo I
B) I y III
C) solo III
D) I y II
E) I, II y III
PREGUNTA 28 :
La sanguina seca (pintura roja) contiene, como pigmento, aproximadamente el 63% en masa de óxido férrico, ¿cuántos mililitros de ácido clorhídrico 2 M se requieren para que todo el pigmento contenido en 10 g de sanguina reacciones totalmente con el ácido?
A) 20
B) 40
C) 79
D) 118
E) 137
PREGUNTA 29 :
Una posible solución a la contaminación relacionada a los gases emanados por los motores de los autos es el uso de celdas de combustible H2-O2. Al respecto, ¿cuáles de las siguientes proposiciones son correctas?
I) En la celda se producen reacciones de oxidación-reducción.
II) La celda produce agua como producto.
III) La celda produce principalmente energía térmica.
A) I y II
B) I y III
C) II y III
D) solo II
E) solo III
PREGUNTA 30 :
Los elementos del grupo 17 de la tabla periódica moderna son conocidos como halógenos (“formadores de sales”). ¿Cuál de los siguientes compuestos corresponde a una sal de un halógeno?
A) NH4NO3
B) K2S
C) NaCl
D) Mg3N2
E) Br2
PREGUNTA 31 :
Se tiene una mezcla de tetróxido de dinitrógeno y de dióxido de nitrógeno en equilibrio, a 0ºC y 1 atm, de acuerdo a la reacción
Si en esas condiciones la presión parcial del N2O4(g) es 0,8 atm, determine el valor de la constante Kc
A) 2,2×10–3
B) 1,1×10–2
C) 5,0×10–2
D) 2,5×10–1
E) 5,0×10–1
PREGUNTA 32 :
Dada la siguiente tabla de constantes de ionización ácida a 25 ºC
¿Cuáles de las siguientes proposiciones son correctas?
I) AℓHBrO le corresponde la base conjugada más estable.
II) HCℓO2 es el ácido más reactivo.
III) La base conjugada de HN3 es N–3 y es la base conjugada más débil.
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
PREGUNTA 33 :
Se tiene un pequeño volumen de cierta muestra líquida y se determina su densidad mediante un método sencillo. Para esto se midió la masa de un vaso de precipitado vacío y seco obteniéndose 12,074 gramos. Luego se vertió en el vaso 5,6 mL de la muestra líquida y la masa medida del vaso y el líquido contenido fue de 17,632 gramos. ¿Cuál es la densidad de la muestra líquida? (kg/m³)
A) 8,83×10²
B) 9,93×10²
C) 1,04×10³
D) 2,09×10³
E) 3,06×10³
PREGUNTA 34 :
Dadas las siguientes proposiciones con respecto a la electrólisis de una solución de ioduro de potasio (KI), ¿cuáles son correctas?
I) Se produce iodo (I2) en el cátodo.
II) La reacción se lleva a cabo de manera espontánea.
III) La solución que rodea al cátodo cambia a fucsia con la adición de fenolftaleína.
Potencial estándar de reducción (V)
A) solo I
B) solo II
C) solo III
D) I y III
E) I, II y III
PREGUNTA 35 :
¿Cuáles de las siguientes moléculas presentan momento dipolar nulo?
A) solo I
B) solo II
C) solo III
D II y III
E) I, II y III
PREGUNTA 36 :
Un recipiente rígido contiene 1000 litros de gas metano (CH4) a 0 °C y una atmósfera. Si se libera el gas hasta que su presión disminuye a la mitad de su valor inicial, manteniendo la misma temperatura, ¿cuántos gramos de metano quedarán en el balón?
R=0,082 atm· L/mol K
Masas atómicas: H=1, C=12
A) 22,3
B) 44,6
C) 357,2
D) 714,5
E) 1429,4
PREGUNTA 37 :
Un estudiante analiza los potenciales de reducción del aluminio y hierro:
De su análisis deduce que el aluminio debería corroerse más fácilmente que el hierro y, siendo así, una lata hecha de aluminio con gaseosa debería corroerse más rápidamente. Por lo tanto, las latas de gaseosa deberían hacerse de hierro. Sin embargo, esto no ocurre así. ¿Cuál es la razón por la cual ese proceso de corrosión no se observa en las latas de aluminio?
A) Debido a la capa de óxido de aluminio (Aℓ2O3) que se forma en la superficie del metal y lo protege.
B) El potencial de oxidación del aluminio es muy bajo.
C) El aluminio es pintado con alguna capa de barniz.
D) Se forma carbonato de aluminio insoluble. Aℓ2(CO3)3, sobre el metal y lo protege.
E) El líquido de una gaseosa no es un medio corrosivo.
PREGUNTA 38 :
La lejía es una solución utilizada en la desinfección y como sacamanchas. Una lejía tiene una concentración al 5% en masa de hipoclorito de sodio (NaCℓO).
Determine la molaridad (mol/L) de un galón de dicha lejía si tiene una densidad de 1,11 g/mL.
Masa molar (NaCℓO)= 74,5 g/mol
A) 0,74
B) 1,11
C) 1,48
D) 2,22
E) 2,96
PREGUNTA 39 :
La ionización del H2S en medio acuoso se produce mediante las siguientes reacciones:
¿Cuál es la concentración molar (mol/L) de los iones H+ en una solución acuosa de H2S 0,1 M?
A) 1,0×10–3
B) 1,0×10–4
C) 1,0×10–5
D) 1,0×10–6
E) 1,0×10–7
PREGUNTA 40 :
¿Cuántos de los siguientes fenómenos presentados en las proposiciones son químicos?
I) Laminación del cobre
II) Oxidación del hierro
III) Evaporación del agua
IV) Fermentación de la uva
V) Disolución del azúcar en agua
A) 1
B) 2
C) 3
D) 4
E) 5
CLAVES-RESPUESTAS : 1)E 2)C 3)D 4)E 5)D 6)C 7)C 8)B 9)D 10)A 11)A 12)B 13)C 14)E 15)C 16)D 17)A 18)C 19)A 20)C 21)E 22)D 23)D 24)A 25)A 26)D 27)E 28)D 29)A 30)C 31)A 32)B 33)B 34)C 35)A 36)C 37)A 38)A 39)B 40)B
SOLUCIONARIO