TERMODINÁMICA EJERCICIOS RESUELTOS PDF – CICLO DE CARNOT – MÁQUINAS TÉRMICAS – PRIMERA Y SEGUNDA LEY
La termodinámica trata acerca de la transformación de energía térmica en energía mecánica y el proceso inverso, la conversión de trabajo en calor.
PREGUNTA 1
PREGUNTA 2
Un gas ideal diatómico se expande adiabáticamente tal que su temperatura disminuye en 400°C. Si el trabajo realizado por el gas es de 16,62 kJ, determine el número de moles del gas.
(R= 8,31 J mol–1 K–1)
A) 8
B) 3
C) 20
D) 2
E) 16
Resolución
Rpta. : "D"
PREGUNTA 3
En una planta liofilizadora de cebolla china, las máquinas térmicas operan según los procesos que se muestran en la figura: proceso 1 - 2, 2 - 3, 3 - 4, 4 - 1.
Estos procesos son, respectivamente:
A) Isobárico, isométrico, adiabático, isotérmico
B) Isobárico, adiabático, isométrico, isotérmico
C) Isométrico, isobárico, isotérmico, adiabático
D) Isobárico, isotérmico, adiabático, isométrico
E) Isométrico, isobárico, adiabático, isotérmico
Resolución
• El proceso 1-2 es isobárico, ya que su presión es constante.
• El proceso 2-3 es isométrico, ya que su volumen es constante.
• El proceso 3-4 es adiabático, ya que al ser una máquina térmica se puede considerar que el proceso se lleva muy rápidamente, por lo que Q= 0.
• El proceso 4-1 es isotérmico, ya que su temperatura es constante.
Rpta. : "A"
PREGUNTA 4
Un gas ideal desarrolla el ciclo termodinámico que se muestra en el diagrama P – V.
Indique verdadero (V) o falso (F) para las siguientes proposiciones.
1. En el proceso a – b aumenta la energía interna.
2. El gas disipa calor en los procesos b – c y c – a.
3. El proceso c – a no es isotérmico.
A) FFV
B) VFV
C) VVF
D) VVV
E) FVF
Resolución
Rpta. : "D"
PREGUNTA 5
La temperatura del reservorio caliente de una máquina térmica bajo un ciclo de Carnot es de 200°C y del reservorio frío es de 50°C. El calor que libera la máquina es de 1000 J. Calcule aproximadamente, en J, el trabajo que realiza la máquina.
A) 564
B) 264
C) 464
D) 164
E) 364
Resolución
Rpta. : "C"
PREGUNTA 7
En el proceso iaf del diagrama, un gas ideal absorbe 50 cal y realiza un trabajo de 20 cal. ¿Qué trabajo realiza el gas en el proceso ibf si absorbe 40 cal?
A) 10 cal.
B) 18 cal.
C) 20 cal.
D) 30 cal.
E) 40 cal.
Resolución
Rpta. : "A"
PREGUNTA 8
En la figura se muestra el ciclo termodinámico realizado por una máquina térmica. Si en cada ciclo se realiza 1kJ de trabajo, el trabajo realizado en el proceso isotérmico, en kJ, es:
A) 0,6
B) 0,8
C) 1,0
D) 1,2
E) 1,5
Resolución
Rpta. : "E"
PREGUNTA 9
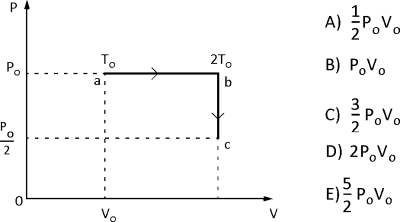
Un gas ideal a la presión P0 y volumen V0 (estado a) se expande isobáricamente hasta duplicar su temperatura (estado b) luego se reduce su presión a la mitad, a volumen constante (estado c). Calcule el trabajo realizado por el gas en todo el proceso.
Rpta. : "B"
PREGUNTA 11
Un gas ideal opera como sustancia de trabajo en un ciclo termodinámico compuesto de dos isócoras y dos isotermas. Si durante la operación el volumen del gas varía 2 veces y su temperatura absoluta varía 3 veces, entonces el rendimiento del gas en el ciclo termodinámico es:
(coeficiente adiabático del gas =1,5 ; Ln2=0,7)
A) 10/61
B) 12/61
C) 14/61
D) 16/61
E) 18/61
Resolución
Rpta. : "C"
PREGUNTA 12
Un mol de un gas ideal se expande adiabáticamente realizando un trabajo de 6000J. ¿Cuál es el cambio de temperatura en grados kelvin del gas después de la expansión?
R=8,314 J/mol.K
A) –441,1
B) –451,1
C) –461,1
D) –471,1
E) –481,1
Resolución
Rpta. : "E"
PREGUNTA 13
La figura muestra 2 kg de argón y 2 kg de nitrógeno molecular, que se encuentran ocupando volúmenes iguales a 0,5m3 cada uno en los recipientes A y B, respectivamente, separados por un pistón sin fricción y no conductor del calor con su entorno. Si la temperatura del argón es de 50°C y se le suministra calor a ambos recipientes hasta conseguir un incremento de temperatura en el argón igual a 200°C, entonces la temperatura final del nitrógeno molecular, en kelvin, es
A) 326,1
B) 336,1
C) 346,1
D) 356,1
E) 366,1
Resolución
Rpta. : "E"
PREGUNTA 14
En un ciclo de Carnot de un gas ideal ( γ=5/3) , se tiene que durante la expansión isotérmica el volumen se duplica y en la expansión adiabática el volumen aumenta en un 25%. Calcule la relación entre la máxima y mínima temperatura en este ciclo
A) (1/4)2/3
B) (3/4)2/3
C) (5/4)2/3
D) (7/4)2/3
E) (9/4)2/3
Resolución
Rpta. : "C"
PREGUNTA 15
Una máquina térmica ideal de gas opera en un ciclo de Carnot entre 227°C y 127°C absorbiendo 6,0×104 cal de la temperatura superior. La cantidad de trabajo, en 103cal, que es capaz de ejecutar esta máquina es:
A) 12
B) 16
C) 20
D) 28
E) 34
Resolución
Rpta. : "A"
PREGUNTA 16
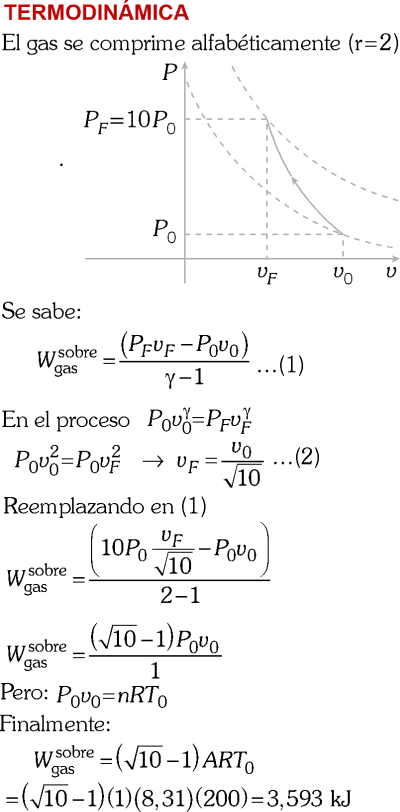
Si un mol de oxígeno que se encontraba inicialmente a la temperatura de 200K, se comprimió adiabáticamente hasta que su presión aumentó en 10 veces respecto a su presión inicial, entonces el trabajo realizado sobre el gas, en kJ, es:
(coeficiente adiabático del gas = 2; R=8,31 J/kg.K)
A) 3593
B) 2789
C) 1645
D) 1745
E) 1845
Resolución
Rpta. : "A"
PRACTICA PROPUESTA
PREGUNTA 1 :
Juan cuida su peso y come nada más que 3000 kcal por día. Al levantar cajas de 3kg hasta una plataforma de 1m de altura, a razón de 10 cajas por minuto por media hora, que porcentaje de la energía que ingirió ha gastado Juan en este trabajo. (1cal =4,18J) suponer que g=10m/s²
A) Más de uno por ciento
B) Mucho más de uno por ciento
C) Menos de un décimo por ciento
D) Alrededor del cincuenta por ciento
E) Faltan datos para calcular el porcentaje
Rpta. : "C"
PREGUNTA 2 :
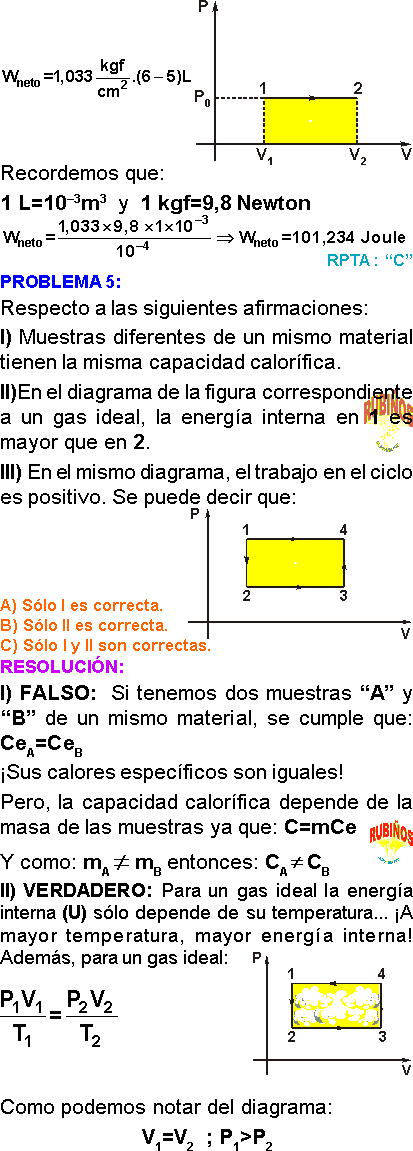
Calcular el trabajo en Joules que realiza un gas ideal cuando se calienta isobáricamente desde los 27°C hasta 87°C , si se encuentra dentro de un recipiente cerrado por un émbolo móvil. El volumen inicial es de 5 litros y la presión atmosférica es 1,033 kg–f/cm².
A) 11,4
B) 112,4
C) 101,2
D) 140
E) 10
Rpta. : "C"
PREGUNTA 3 :
Un litro de Argón, contenido en un cilindro con un pistón, se expande contra la presión atmosférica hasta que alcanza un volumen triple.
¿Qué trabajo ha sido realizado por el gas?.
(Considere 1 atmósfera =10⁵ N/m²)
A) 200 joules
B) 300 joules
C) 450 joules
D) 350 joules
Rpta. : "A"
PREGUNTA 4 :
Se calienta un mol de gas oxígeno desde una temperatura de 20°C y presión de 1 atm, hasta una temperatura de 100°C. Suponiendo que el gas oxígeno es un gas ideal determine (en J) el calor que deberá suministrarse si durante el calentamiento se mantiene constante:
(a) el volumen, (b) la presión.
A) 1662; 2466,6
B) 1422; 1682,8
C)1652; 2326,8
D) 1660; 2400
E) 1720; 1920
Rpta. : "C"
PREGUNTA 5 :
Cuando un gas ideal se expande adiabáticamente, ¿cuál de las siguientes proposiciones no es correcta?
A) La temperatura del gas disminuye.
B) El gas realiza trabajo.
C) Es necesario suministrar calor al gas para que realice trabajo.
D) La energía interna del gas disminuye.
E) La presión del gas disminuye.
Rpta. : "C"
PREGUNTA 6 :
Un sistema sufre un proceso en el cual absorbe 50 calorías de calor y se expande realizando un trabajo de 319 joules. ¿Cuál es la variación de la energía interna en joules que experimentó el sistema?
(1 caloría =4,18 joules)
A) 0
B) 100
C) –120
D) 120
E) –110
Rpta. : "E"
PREGUNTA 7 :
Un gas ideal, contenido en un cilindro que tiene un pistón movible, tiene una presión p=400kPa. Se le proporciona 20 kJ de calor y se expande isobáricamente hasta alcanzar un volumen igual a 1,5 veces su volumen inicial. Su energía interna aumenta en 10kJ en este proceso.
Determine el volumen inicial del gas en m³.
A) 0,01
B) 0,02
C) 0,03
D) 0,04
E) 0,05
Rpta. : "E"
PREGUNTA 8 :
Se comprime adiabáticamente un mol de gas monoatómico, efectuando sobre éste un trabajo de 100 kJ. ¿En cuántos grados Kelvin aumentó la temperatura del gas?
A) 12,5
B) 22,5
C) 920,5
D) 1035
E) 8022
Rpta. : "E"
PREGUNTA 9 :
En un proceso termodinámico isobárico un gas monoatómico experimenta una expansión de manera que la presión se mantiene en 80kPa durante todo el proceso, si su volumen se incrementa de 1m³ a 3m³, determine (en kJ) el calor entregado al gas.
A) 100
B) 200
C) 300
D) 400
E) 480
Rpta. : "D"
PREGUNTA 10 :
Un gas que inicialmente se encuentra a P0=16Pa y V0=2m³, se expande de tal manera que su presión varía de acuerdo a la ecuación: P=20 – 2V.
Calcular el trabajo desarrollado por el gas hasta que su volumen es 8m³.
A) 9J
B) 12J
C) 18J
D) 16J
E) 60J
Rpta. : "E"
PREGUNTA 11 :
Un recipiente contiene 320g de oxígeno a la temperatura de 20°C. Determine la cantidad de calor que se le debe suministrar (en kJ) para elevar su temperatura hasta 220°C manteniendo la presión constante (Cp=7R/2)
A) 230,1
B) 124,8
C) 18,6
D) 58,17
E) 63,26
Rpta. : "D"
PREGUNTA 12 :
Indicar la expresión incorrecta:
A) El calor es la energía que se intercambia entre dos cuerpos en contacto debido a la diferencia de temperaturas.
B) El calor puede transmitirse en forma espontánea de un cuerpo caliente a otro frío y viceversa.
C) En un proceso isotérmico realizado por un gas ideal, si se hace trabajo sobre el gas es necesario que el gas entregue calor a los alrededores para mantener la temperatura constante.
D) La primera ley de la Termodinámica es la ley de conservación de la energía.
E) Una máquina de Carnot de eficiencia 100% necesitaría de un reservorio de calor frío a cero grados Kelvin.
Rpta. : "B"
PREGUNTA 13 :
Un gas ideal realiza un ciclo de Carnot. La expansión isotérmica ocurre a 250°C y la compresión isotérmica tiene lugar a 50°C. Si el gas absorve 1200J de calor durante la expansión isotérmica, entonces el trabajo neto en Joules, realizado por el gas en cada ciclo es: (no considere decimales)
A) 228J
B) 308
C) 720
D) 459
E) 20
Rpta. : "D"
PREGUNTA 14 :
Un reservorio térmico a 1000K, transfiere 125 400J de calor a una máquina térmica de Carnot, durante un ciclo termodinámico. Si el trabajo neto de la máquina térmica es 2×10⁴J, la temperatura del reservorio térmico de baja temperatura en K, aproximadamente, es:
A) 410
B) 644
C) 716
D) 841
E) 886
Rpta. : "D"
PREGUNTA 15 :
Una máquina térmica de Carnot recibe 1200 kJ/min de calor desde un foco térmico que está a 727°C, y rechaza calor a un sumidero térmico que está a 17°C.
Determinar la potencia neta que entrega la máquina (kW).
A) 28,0
B) 19,5
C) 852
D) 14,2
E) 10,8
Rpta. : "D"
PREGUNTA 16 :
Una máquina térmica que realiza un trabajo de 100 kJ/ciclo, devuelve 25 kJ de calor a la fuente fría.
¿Cuál es la eficiencia (en %)?
A) 20
B) 40
C) 60
D) 80
E) 90
Rpta. : "D"
PREGUNTA 17 :
Una máquina térmica de Carnot absorve calor de una fuente caliente que se encuentra a 227°C y tiene una eficiencia de 32%. ¿Cuánto debe variar la temperatura (en K) de la fuente caliente para que la eficiencia se eleve a 43,33%?
A) 20
B) 100
C) 200
D) 50
E)–20
Rpta. : "B"
PREGUNTA 18 :
Una máquina térmica experimenta un ciclo de Carnot, recibe de un foco a 527°C, 1000J y realiza un trabajo, cediendo una cierta cantidad de calor a un foco frío el cual se encuentra a 27°C. Determine el trabajo realizado por el motor y su eficiencia.
A) 625J; 62,5%
B) 375J; 60%
C) 1 000J; 100%
D) 625J; 80%
Rpta. : "A"
PREGUNTA 19 :
Un gas ideal con volumen inicial de 2m³ y una presión de 500Pa se expande isobáricamente y alcanza un volumen de 4m³ y una temperatura de 120K. Luego se enfría a volumen constante hasta que su temperatura es de 60K. Finalmente se expande a presión constante hasta un volumen de 8m³. Determine el trabajo total , en joules, realizado por el gas en este proceso.
A) 1,00×10³
B) 1,50×10³
C) 2,00×10³
D) 2,50×10³
E) 3,00×10³
Rpta. : "C"
PREGUNTA 20 :
Una máquina térmica trabajando con un rendimiento de 50% absorve 300cal de una fuente de calor , en cada ciclo y desprende una cantidad Q de calor hacia un sumidero a la temperatura de 250K . Hallar Q y la temperatura de la fuente de calor
A)150 cal; 500K
B) 130 cal; 600K
C) 140 cal; 400K
D)160 cal; 300K
Rpta. : "A"
PREGUNTA 20 :
Una máquina térmica ideal opera entre dos fuentes de calor, cuyas temperaturas son respectivamente 127°C y 27°C. Hallar el trabajo que realiza la máquina, si absorve 600 calorías de la fuente de alta temperatura.
A) 1,9×10² cal
B) 4,74×10² cal
C) 2,0×10² cal
D) 1,5×10² cal
E) 2,3×10² cal
Rpta. : "D"
PREGUNTA 21 :
Una máquina térmica cuyo rendimiento es 20% se acopla a otra máquina de rendimiento 25%, de manera que el calor liberado por la primera es absorbido por la segunda. Halle la eficiencia (en %) del sistema de máquinas.
A) 5
B) 20
C) 25
D) 40
E) 50
Rpta. : "D"
PREGUNTA 22 :
Una máquina de Carnot trabaja entre dos isotermas TA=27°C y TB=–73°C si recibe 120 cal de la fuente caliente durante cada ciclo, ¿cuánto calor (en cal) cede en cada ciclo a la fuente fría?
A) 50
B) 180
C) 90
D) 120
E) 80
Rpta. : "E"
PREGUNTA 23 :
El calor que absorbe una máquina térmica es 3 veces el trabajo que realiza.
¿Qué fracción (en %) del calor absorbido es liberado hacia el depósito frío?.
A) 33
B) 45
C) 52
D) 67
E) 75
Rpta. : "D"
PREGUNTA 24 :
Indique la veracidad (V) o falsedad (F) de las siguientes proposiciones:
I) Usar el calor que rechaza una máquina térmica para alimentar otra máquina térmica transgrede la segunda ley.
II) Según la segunda ley todas las máquinas ideales tienen la misma eficiencia.
III) Según la segunda ley solo las máquinas térmicas ideales tienen eficiencia del 100%.
A) VVV
B) VFV
C) VVF
D) FVF
E) FFF
Rpta. : "E"
EJERCICIO 1
Señale la proposición verdadera respecto al ciclo de Carnot.
A) Durante la expansión isotérmica el sistema pierde calor.
B) Durante la expansión adiabática la energía interna aumenta.
C) Durante la compresión isotérmica el sistema gana calor.
D) Durante la compresión adiabática, la energía interna aumenta.
E) El área encerrada por el ciclo equivale a la variación de la energía interna de todo el ciclo.
EJERCICIO 2
Sobre la Primera ley de la Termodinámica indique las proposiciones verdaderas (V) o falsas (F).
I) Q – W representa el cambio de energía interna del sistema.
II) La primera ley se aplica se aplica a todo proceso en la naturaleza que comienza en un estado de equilibrio y termina en otro.
III) En un proceso adiabático la energía interna de un sistema aumenta exactamente en la cantidad de trabajo efectuada sobre el sistema.
A) VFF
B) FFV
C) VVV
D) FVF
E) VFV
EJERCICIO 3
Señale la proposición verdadera respecto al ciclo de Carnot.
A) Durante la expansión isotérmica el sistema pierde calor.
B) Durante la expansión adiabática la energía interna aumenta.
C) Durante la compresión isotérmica el sistema gana calor.
D) Durante la compresión adiabática la energía interna aumenta.
E) El área encerrada por el ciclo equivale a la variación de la energía interna de todo el ciclo.
EJERCICIO 4
Considerando solo los procesos termodinámicos isocórico, isobárico, isotérmico y adiabático para un gas ideal, indique si las siguientes proposiciones son verdaderas (V) o falsas (F) y marque la alternativa correcta.
I) En un proceso isocórico la variación de energía interna del gas es nula.
II) En un proceso de compresión adiabática la temperatura del gas disminuye
III) En un proceso isobárico la presión del gas es constante.
A) VFF
B) FFV
C) VVV
D) FVF
E) VFV
EJERCICIO 5
Indique las proposiciones correctas respecto de la segunda Ley de termodinámica.
I) Se fundamenta en la primera ley de la termodinámica.
II) Es imposible construir una máquina térmica que transforme íntegramente todo el calor que recibe en trabajo.
III) Sostiene que si es posible construir una máquina térmica cuya eficiencia sea del 100%.
A) Sólo I
B) Sólo II
C) Sólo III
D) Sólo I y II
E) Sólo II y III
EJERCICIO 6
Indique las proposiciones correctas respecto de la segunda Ley de Termodinámica.
I) Se fundamenta en la conservación de energía.
II) Propone que solo la máquina de Carnot es 100% eficiente.
III) Sostiene que no es posible construir una máquina térmica 100% eficiente.
A) Sólo I
B) Sólo II
C) Sólo III
D) Sólo I y II
E) Sólo II y III
EJERCICIO 7
Determine la verdad (V) o falsedad (F) de las siguientes proposiciones:
I) Una máquina térmica es aquél sistema que permite transformar energía térmica en cualquier otra forma de energía.
II) Toda máquina térmica opera siempre entre dos focos térmicos.
III) En una máquina térmica se cumple el principio de conservación de energía.
A) VFF
B) FFV
C) VVV
D) FVV
E) VFV
EJERCICIO 8
En relación a las siguientes proposiciones sobre las máquinas térmicas, indique verdadero (V) o falso (F) y marque la alternativa correspondiente
I) Convierten parte del calor en trabajo mecánico
II) Operan según ciclos termodinámicos.
III) Son 100% eficientes
A) VFF
B) FFV
C) VVV
D) FVF
E) VVF
APRENDIZAJES DESEADOS
☛ Estudiar el principio de conservación de la energía en su forma mas general.
☛ Conocer la forma que toma este principio aplicado a los diversos procesos termodinámicos.
☛ Utilizar la aplicación de este principio en las llamadas maquinas térmicas.
Puesto que casi toda la energía disponible de la materia prima se libera en forma de calor, resulta fácil advertir por qué la termodinámica juega un papel tan importante en la ciencia y la tecnología.
Veremos 2 leyes básicas que deben obedecerse cuando se utiliza energía térmica para realizar trabajo.
La primera ley es simplemente volver a postular el principio de la conservación de la energía.
La segunda ley impone restricciones sobre el uso eficiente de la energía disponible.
SISTEMA TERMODINÁMICO
Es aquella porción de materia que puede considerarse limitada por una superficie cerrada real o imaginaria. La región no incluida en el sistema constituye el exterior o alrededores o ambiente.
Los desafíos que hoy en día experimenta la población mundial tiene que ver principalmente con la falta de alimentos, escasez de espacios para vivir, falta de agua, contaminación de los espacios acuíferos, elevados costos de los combustibles fósiles, calentamiento global de la tierra, contaminación ambiental, etc
Desafortunadamente todos estos eventos afectan nuestro país, por otro lado todos estos sucesos involucran al hombre y son consecuencia de la forma como administra los diferentes recursos Una de las ciencias dentro de la física que establece distintas leyes para tener un mejor entendimiento de los procesos que modifican en cierta medida el entorno del ser humano es la TERMODINÁMICA la cual deriva de dos vocablos griegos thermós ( y dýnamis ( fuerza)
El estudio teórico y el desarrollo de diversas máquinas dieron origen a esta ciencia durante la revolución Industrial La Termodinámica se define básicamente como una ciencia que se encarga del estudio de las leyes que gobiernan la transformación de energía La dirección en la cual el calor fluye y la disponibilidad exergía de la energía para hacer trabajo.
Es importante señalar que estos procesos de transformación de energía pueden estar acompañados d e cambios físicos y químicos. La termodinámica permite el análisis de procesos naturales y artificiales por ejemplo , todo organismo vivo requiere un suministro continuo de energía para mantenerse vivo. Una gran parte de los dispositivos bioquímicos de las células se encargan de adquirir y transformar energía.
Casi todas las actividades realizadas por el ser humano involucran transformaciones de energía Para su estudio, la termodinámica se apoya en la ley cero, la primera, la segunda y la tercera ley de la termodinámica.
Entre las aplicaciones de la física que pueden ser analizadas por la termodinámica destacan: plantas de generación de potencia eléctrica , sistemas de calefacción y de refrigeración , celdas de combustible, aerogeneradores , centrales maremotrices , turbinas , Procesos de combustión , automóviles y transformaciones de Energía de diversos sistemas biológicos , entre otras