UNI 2025-2 TERCERA PRUEBA RESUELTA RESPUESTAS FÍSICA QUÍMICA INGRESO UNIVERSIDAD PDF CIENCIAS
CLAVES – RESPUESTAS
1)B 2)C 3)A 4)B 5)B 6)C 7)A 8)D 9)C 10)E 11)E 12)D 13)B 14)C 15)C 16)C 17)D 18)C 19)E 20)A 21)C 22)A 23)E 24)E 25)E 26)D 27)A 28)E 29)E 30)E 31)A 32)E 33)B 34)B 35)B 36)E 37)D 38)D 39)E 40)B
- CLIC AQUÍ Ver 3ra PRUEBA UNI 2025 II PDF
- Ver SOLUCIONARIO 3ra PRUEBA UNI 2025 II PDF
- Ver CLAVES– RESPUESTAS
PREGUNTA 1
Sean los vectores:
A) 2
B) 5
C) 2√2
D) 2√5
E) 4√2
Resolución
Clave D
PREGUNTA 2
Una partícula realiza un MRU a lo largo del eje X. En t=0 s pasa por la posición 5î m y en un intervalo de tiempo de 3s el vector desplazamiento es – 7,5î m. Determine la posición de la partícula (en m) cuando t=10 s.
A) – 20î
B) – 10î
C) 10î
D) 20î
E) 30î
Resolución
Clave A
PREGUNTA 3
Al lanzar un proyectil con una velocidad inicial v0, que forma un ángulo de 37° con el eje X, el alcance horizontal es de 100m. Calcule el nuevo alcance (en m) si el ángulo que forma la velocidad inicial es de 53° y se mantiene la misma rapidez.
A) 60
B) 75
C) 100
D) 120
E) 125
Resolución
Clave C
PREGUNTA 4
Una partícula gira con MCU de tal modo que da una vuelta en 10s. Calcule aproximadamente el radio de giro (en cm) si para recorrer 20 cm de arco emplea 5 s.
A) 2,89
B) 3,91
C) 4,12
D) 5,23
E) 6,37
Resolución
Clave E
PREGUNTA 5
Un bloque de 6 kg se suelta en el punto A y luego pasa por el punto B con una rapidez de 20 m/s. Determine el trabajo realizado por la fuerza de fricción (en J) desde el punto A hasta el punto B.
Considere g= 9,81 m/s2.
A) – 471,5
B) – 371,5
C) – 281,5
D) – 271,5
E) – 171,5
Resolución
Clave D
PREGUNTA 7
Un carrito desciende por un plano inclinado 53° respecto a la horizontal con aceleración constante a , tal como se muestra en la figura. Si la masa m, suspendida del techo del carrito con una cuerda de masa despreciable, forma un ángulo de 37° con la perpendicular al plano inclinado, determine el valor aproximado de la magnitud de la aceleración a (en m/s2).
Considere g=9,81m/s2
A) 2,0
B) 3,4
C) 4,5
D) 5,0
E) 5,5
Resolución
Clave B
PREGUNTA 8
Calcule aproximadamente la potencia (en mW) que disipa un cable delgado de oro de 10 m de longitud y 1,0 mm de radio, cuando fluye una intensidad de corriente eléctrica de 0,10 A. Considere la resistividad eléctrica del oro igual a 2,44 ×10–8 Ω ∙ m.
A) 0,28
B) 0,38
C) 0,58
D) 0,78
E) 0,98
Resolución
Clave D
PREGUNTA 9
Calcule la masa mínima aproximada (en g) de vapor de agua que se necesita para descongelar 400 g de hielo a 0 °C y llevarlo hasta 100°C (sin convertirse en vapor).
Lf= 333 kJ/kg
Lv=2260 kJ/kg
c=4,18 kJ/kg.K
A) 102,9
B) 112,9
C) 122,9
D) 132,9
E) 142,9
Resolución
Clave D
PREGUNTA 10
Sobre una superficie de cobre inciden fotones con longitud de onda λ. Si el potencial de frenado del cobre es de 1,3 V, calcule aproximadamente λ (en nm).
Considere: La función trabajo del cobre igual a 4,7 eV
1 eV=1,602×10–19 J
h=6,626×10–34 J · s
c =3×108 m/s
A) 148
B) 207
C) 347
D) 448
E) 557
Resolución
Clave B
PREGUNTA 11
Una carga eléctrica q=2mC se mueve desde el punto A hasta el punto B dentro de un campo eléctrico uniforme E, tal como se muestra en la figura.
Calcule el trabajo realizado por el campo eléctrico sobre la carga eléctrica (en mJ).
A) 40
B) 50
C) 70
D) 80
E) 90
Resolución
Clave D
PREGUNTA 12
Calcule aproximadamente la masa de un gas oxígeno (en g) que se encuentra en el interior de un globo de forma esférica de 15 cm de radio a una presión y temperatura de 1 atm y 20 °C. Considere: 1 atm =101×103 Pa; R=8,31J/mol·K; masa molar de oxígeno = 16 g/mol.
A) 3,4
B) 6,4
C) 9,4
D) 11,4
E) 14,4
Resolución
Clave C
PREGUNTA 13
Los valores de las longitudes de onda de la radiación electromagnética emitida por un cuerpo se encuentran entre 380 nm y 780 nm.
Calcule el valor aproximado de la energía máxima (en eV) que puede tener un fotón.
h=4,1×10–15 eV · s
c=3,0×108 m/s
A) 1,24
B) 2,24
C) 3,24
D) 4,24
E) 5,24
Resolución
Clave C
PREGUNTA 14
Un electrón cuya velocidad es
Calcule aproximadamente el radio de curvatura (en mm) de la trayectoria que describe el electrón. Considere la carga del electrón igual a 1,6 ×10–19 C y la masa del electrón igual a 9,11×10–31 kg.
A) 1,7
B) 2,3
C) 2,8
D) 3,9
E) 5,4
Resolución
Clave C
PREGUNTA 15
Un protón se mueve en una región donde hay un campo magnético de magnitud 1,75 T y orientado hacia al eje Z positivo. La rapidez del protón es 4,46×106m/s moviéndose hacia el eje X positivo.
Calcule el valor aproximado de la magnitud de la fuerza magnética (en N) que actúa sobre el protón.
Carga del protón: 1,6×10–19C
A) 4,45×10–13
B) 8,25×10–13
C) 1,25×10–12
D) 2,15×10–11
E) 3,15×10–10
Resolución
Clave C
PREGUNTA 16
Calcule la resistencia R (en Ω) tal que la potencia disipada por todo el circuito sea de 3W.
A) 10
B) 20
C) 30
D) 40
E) 50
Resolución
Clave A
PREGUNTA 17
La ecuación y=3sen(x –10t), con unidades en el Sistema Internacional, representa a una onda que se propaga a través de una cuerda tensa. Si la densidad lineal de la cuerda es μ= 1 g/m, calcule la potencia media que propaga la onda (en W).
A) 3
B) 3,5
C) 4
D) 4,5
E) 9
Resolución
Clave D
PREGUNTA 18
Un trozo de madera con 0,60m de largo, 0,25m de ancho y 0,08m de espesor, cuya densidad es 600kg/m3, flota parcialmente en la superficie del agua. Determine aproximadamente el volumen (en unidades de 10–4 m3) de un trozo de plomo (ρplomo=11300 kg/m3) que debe sujetarse en la base de la madera para hundirla de modo que la cara superior de la madera se encuentre al mismo nivel del agua.
Considere: ρagua=1000 kg/m3
A) 3,2
B) 3,9
C) 4,7
D) 5,6
E) 6,7
Resolución
Clave C
PREGUNTA 19
Un planeta tiene una masa igual a 4 veces la masa de la Tierra y el mismo radio. Calcule a qué altura de la superficie de dicho planeta la aceleración de la gravedad es igual a g.
g: aceleración de la gravedad en la superficie de la Tierra.
R: radio de la Tierra.
A) R/4
B) R/2
C) R
D) 2R
E) 4R
Resolución
Clave C
PREGUNTA 20
Una partícula se aproxima con velocidad constante, a lo largo del eje principal, al vértice de una lente convergente cuya distancia focal es de 20 cm. Si el objeto pasa de una distancia a la lente de 100 cm a otra de 30 cm en 5 s, calcule la rapidez media (en cm/s) de la imagen.
A) 5
B) 7
C) 9
D) 11
E) 13
Resolución
Clave B
QUÍMICA
PREGUNTA 21
La lluvia ácida se debe principalmente a la presencia del ácido sulfúrico (H2SO4) y ácido nítrico (HNO3) en el agua de lluvia.
Señale la alternativa correcta que contiene a los contaminantes primarios que generan respectivamente estos ácidos.
A) SO2 y NO3
B) SO3 y NO3
C) SO2 y N2O
D) SO3 y N2O5
E) SO2 y NO2
Resolución
CONTAMINACIÓN AMBIENTAL
La lluvia ácida contiene ácidos corrosivos como el ácido sulfúrico, H2SO4, y el ácido nítrico, HNO3. Estos ácidos son contaminantes secundarios que se forman por diversas reacciones a partir de los contaminantes primarios de la atmósfera. Los contaminantes primarios que generan la lluvia ácida son el óxido de azufre (SO2) y el óxido de nitrógeno (NO2).
Clave E
PREGUNTA 22
En la construcción de un laboratorio de química, encontramos diferentes materiales; por ejemplo, hormigón, clavos de acero, alambres de cobre, agua y andamios de aluminio. Respecto al texto, determine si la proposición es verdadera (V) o falsa (F).
I) Se mencionan 3 sustancias y 2 mezclas.
II) El agua, H2O, es una sustancia heterogénea.
III) El cobre y el aluminio son sustancias elementales.
Marque la secuencia correcta.
A) VFV
B) FFV
C) VFF
D) VVV
E) FFF
Resolución
MATERIA
I) VERDADERO
Mezclas: hormigón y acero Sustancias: alambres de cobre, andamios de aluminio y agua
II) FALSO
El H2O es una sustancia homogénea.
III) VERDADERO
El cobre (Cu) y aluminio (Al) son sustancias simples o elementales.
Clave A
PREGUNTA 23
Respecto a los orbitales atómicos del hidrógeno, determine si la proposición es verdadera (V) o falsa (F).
I) El orbital 3s tiene mayor tamaño que el orbital 2s.
Il) Los orbitales 2s y 3px son degenerados, ya que tienen igual energía.
III) Solo existe el orbital 1s, donde se encuentra su único electrón.
Marque la secuencia correcta.
A) FVF
B) VVF
C) FVV
D) VFF
E) VFV
Resolución
ESTRUCTURA ELECTRÓNICA
I) VERDADERO
Se cumple que a mayor nivel, mayor tamaño, por lo tanto, tamaño: 3s > 2s
II) FALSO
Los orbitales degenerados son aquellos que pertenecen a un mismo subnivel. Los orbitales 2s y 3px pertenecen a subniveles diferentes.
III) FALSO
En el átomo de hidrógeno, existen los orbitales 1s, 2s, 2p, etc., pero solo el subnivel 1s está ocupado con su único electrón.
Clave D
PREGUNTA 25
Respecto al valor de la constante de equilibrio químico:
I) La expresión de la constante de equilibrio para una reacción escrita en un sentido, es el recíproco de la correspondiente a la reacción escrita en el sentido contrario.
II) La constante de equilibrio para cualquier reacción no varía con la temperatura.
III) El valor numérico de la constante de equilibrio varía cuando se introduce un catalizador en el sistema en equilibrio.
Son correctas:
A) Solo I
B) Solo II
C) Solo III
D) I y II
E) I y III
Resolución
EQUILIBRIO QUÍMICO
Respecto a las proposiciones relacionadas con la constante de equilibrio de una reacción:
I. (V) cuando se cambia de sentido a una reacción, los productos se convierten en reactantes, por lo que la expresión de la constante de equilibrio se hace la reciproca con respecto a la inicial.
II. (F) es importante recalcar que el único factor que varía la constante de equilibrio es la temperatura. Si la reacción es endotérmica, el aumentar la temperatura, aumentará la Keq. Si la reacción es exotérmica, al aumentar la temperatura, disminuirá la Keq.
III. (F) la adición de un catalizador la no varía el valor numérico de la constante de equilibrio, a una temperatura específica.
Clave A
PREGUNTA 26
Según la distribución de los elementos químicos en la tabla periódica, ¿cuántas de las siguientes propiedades periódicas aumentan conforme aumenta el número atómico en un periodo?
I) electronegatividad
II) afinidad electrónica
III) potencial de ionización
IV) carácter no metálico
A) 0
B) 1
C) 2
D) 3
E) 4
Resolución
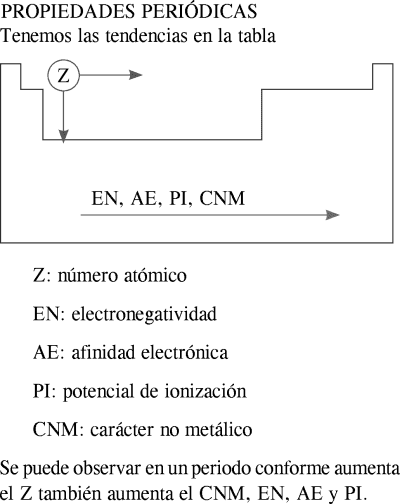
PROPIEDADES PERIÓDICAS
Las propiedades químicas de los elementos químicos varían de forma periódica a lo largo de la tabla periódica. En general, podemos plantear el siguiente esquema para visualizar la variación periódica de las propiedades químicas.
Según las flechas, aumenta lo siguiente:
• energía de ionización
• afinidad electrónica
• electronegatividad
• carácter no metálico
Clave E
PREGUNTA 27
Para las siguientes proposiciones de acuerdo a la reacción adjunta en equilibrio, a 25°C
I) La introducción de un catalizador desfilará la reacción hacia la derecha.
II) Si aumenta la temperatura el valor de la constante de equilibrio aumentará.
III) La disminución del volumen del reactor favorecerá a los productos.
Son correctos
A) solo I
B) solo II
C) solo III
D) I y III
E) II y III
Resolución
EQUILIBRIO QUÍMICO – PRINCIPIO DE LE CHATELIER
I. Incorrecto
la introducción de un catalizador dentro de un sistema de reacción en equilibrio, no modifica el sentido de la misma, solo hace que se alcance más rápido el equilibrio.
II. Correcto
el incremento de la temperatura de una reacción endotérmica, en el sistema de equilibrio, hará que este se desplace hacia la derecha, por lo tanto, el valor de Keq aumentará.
III. Incorrecto
la disminución del volumen hace que la presión del sistema aumente, pero como el número de moles de reactantes y productos son iguales, este efecto no alterará el equilibrio.
Clave B
PREGUNTA 28
Una de las razones por la que se promueve el uso de tecnologías limpias es que evitan el daño al medio ambiente. De las siguientes proposiciones:
I) el uso de refrigerantes que no consuman compuestos clorofluorocarbonados
II) el reciclaje de desechos orgánicos
III) el uso de lámparas de bajo consumo
Indique cuáles involucran el uso de tecnologías limpias para evitar el deterioro de la capa de ozono.
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
Resolución
CONTAMINACIÓN AMBIENTAL
Preguntan qué alternativa propone una tecnología para evitar el deterioro de la capa de ozono. La capa de ozono se encuentra en la estratósfera, el cual es un filtro natural de la radiación ultravioleta (principalmente las de alta energía o baja longitud de onda). Esta capa se va deteriorando por acción química de sustancias como:
• Clorofluorocarbonos (CFC), procedentes de los refrigerantes y aerosoles (freones como el CF2Cl2 que genera cloro atómico).
• Halones como el CF3Br y bromo metilo (CH3Br, que libera bromo).
• Monóxido de nitrógeno (NO) emitidos en humos de aviones.
Luego de analizar las proposiciones, encontramos que la proposición I sugiere evitar el deterioro de la capa de ozono usando refrigerantes que no consuman CFC.
Clave A
PREGUNTA 29
En una celda electroquímica ocurre la siguiente reacción redox:
A) – 0,15
B) +0,15
C) +0,30
D) – 0,30
E) +1,40
Resolución
Clave B
PREGUNTA 30
El niquelado es un proceso utilizado con la finalidad de proteger a piezas metálicas contra la corrosión, teniendo el valor agregado de un mejor acabado.
Calcule la masa (en gramos) de níquel depositada sobre una placa metálica, si ella se sumerge dentro de una celda electrolítica que contiene una solución acuosa NiCℓ2, por la cual pasa por una corriente de 5 A durante 10 minutos.
Datos:
Masa atómica: Ni=58,7
1F=96 500C
A) 0,03
B) 0,91
C) 1,25
D) 1,50
E) 2,00
Resolución
Clave B
PREGUNTA 31
¿En cuál de los siguientes casos, el gas mencionado se comportará más cercanamente a un gas ideal? Masas atómicas: H=1; l=127
A) H2(g) a 1 atm de presión y temperatura ambiente.
B) Hl(g) a 1 atm de presión y temperatura ambiente.
C) H2(g) a 10 atm de presión y temperatura ambiente.
D) Hl(g) a 10 atm de presión y temperatura ambiente.
E) I2(g) a 1 atm de presión y temperatura ambiente.
Resolución
ESTADO GASEOSO
Los gases reales se comportan como ideales cuando están a bajas presiones y altas temperaturas. En el caso del H2(g) es una molécula apolar muy pequeña donde las FIM son mínimas; por ello se comporta como ideal.
Clave A
PREGUNTA 32
Dada la siguiente reacción química
2NH3(g) ⇄ N2(g) + 3H2(g)
con constante de equilibrio Kc=0,83 a 375 °C. Se establece las siguientes proposiciones:
I) La constante Kp, es igual a la constante Kc.
II) Si se adiciona un catalizador al sistema en equilibrio, la reacción se desplaza hacia la izquierda.
III) Al duplicar el volumen del sistema en equilibrio, la reacción se desplaza hacia la derecha.
Indique la alternativa correcta.
A) solo II
B) solo III
C) l y ll
D) I y III
E) II y III
Resolución
Clave B
PREGUNTA 33
El hipoclorito de sodio (NaCℓO) es un compuesto muy utilizado para la desinfección del agua potable. Después de determinar si las proposiciones son verdaderas (V) o falsas (F).
I) La masa molar del NaClO es 74,5u.
II) Un mol de NaCℓO tiene una masa de 7,45g.
III) Una masa de 74,5g de NaCℓO contiene 6,022×1023 unidades fórmulas de dicho compuesto.
Dato: Masa atómica: O=16; Na=23; Cℓ=35,5
Marque la alternativa correcta.
A) VVV
B) VFV
C) FFF
D) FFV
E) FVV
Resolución
Clave D
PREGUNTA 34
Para realizar un proceso de electrodeposición en un objeto, este se introduce en una solución que posee un catión metálico divalente durante 1000s con una corriente de 5A, depositándose 1,53 g del metal. Determine qué metal se deposita en el objeto.
Masas atómicas:
Ni = 59; Cu = 63,5; Zn = 65; Cr= 52; Fe=56
A) Fe
B) Cu
C) Zn
D) Ni
E) Cr
Resolución
Clave D
PREGUNTA 35
La solubilidad (S) del KNO3 es:
¿Cuál es la masa (en gramos) de KNO3 que cristalizará al enfriar 765g de solución saturada de KNO3 desde 75°C a 25°C?
A) 402
B) 361
C) 351
D) 328
E) 296
Resolución
Clave C
PREGUNTA 36
El vinagre comercial usualmente contiene un 5% masa/volumen de ácido acético (CH3COOH). Calcule la molaridad (en mol/L) del ácido acético en el vinagre.
Datos:
Masas atómicas:
H = 1, C =12, O=16
A) 0,042
B) 0,083
C) 0,420
D) 0,830
E) 1,200
Resolución
Clave D
PREGUNTA 37
Calcule el grado de ionización de una solución de ácido nitroso, HNO2(ac) 0,2M.
Dato: Ka(HNO2)=4,5×10 –4
A) 0,0095
B) 0,0200
C) 0,0475
D) 0,1000
E) 0,2000
Resolución
Clave C
PREGUNTA 38
Con respecto a la geometría y polaridad molecular:
I) El agua y el trióxido de azufre, SO3, tienen la misma geometría molecular.
II) El amoniaco, NH3, es una molécula tetraédrica, mientras que el tetracloruro de carbono, CCl4, tiene geometría plana trigonal.
III) El BF3 y BeCl2 son moléculas apolares.
Datos: Números atómicos:
H = 1; Be = 4; B = 5; C = 6; N= 7; O = 8; F = 9; S = 16; Cl = 17
Indique la alternativa correcta.
A) solo I
B) solo II
C) solo III
D) I y III
E) I, II y III
Resolución
Clave C
PREGUNTA 39
La fenacetina es un compuesto derivado del benceno y es utilizado como analgésico. Respecto a su estructura:
indique la alternativa correcta.
A) El anillo aromático presenta 3 enlaces sigma.
B) El grupo funcional amida contiene 1 enlace pi.
C) La fenacetina presenta 3 enlaces pi.
D) El anillo aromático presenta 2 enlaces pi.
E) La fenacetina presenta 8 enlaces sigma.
Resolución
Clave B
PREGUNTA 40
Algunas penicilinas comunes son la amoxicilina y la penicilina G, cuyas estructuras se presentan a continuación:
Dadas las siguientes proposiciones respecto a las estructuras mostradas:
I) En una estructura aparece la función alcohol y en la otra no.
II) En ambas estructuras aparece la función aldehído.
III) Una estructura contiene una amina primaria y la otra no.
Indique la alternativa correcta.
A) solo I
B) solo II
C) solo III
D) I y II
E) I, II y III
Resolución
Clave C